摘要:4.根据引起水硬度的离子结合阴离子种类的不同.软化硬水的方法不同.下列各反应不属于硬水软化的是 ( ) A.MgCO3 + H2O Mg(OH)2 + CO2 B.Mg(HCO3)2 MgCO3 + CO2 + H2O C.2NaR + Ca2+ == CaR2 + 2Na+ D.向水中投入明矾Al3+ + 3H2O Al(OH)3+ 3H+
网址:http://m.1010jiajiao.com/timu3_id_314960[举报]
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。

(1)写出C原子的电子排布式____,D元素在周期表中的位置是____。
(2)写出A单质与水反应的离子化学方程式为________。
(3)A与D形成的化合物的电子式为____,溶于水后溶液的pH____7(填“大于”、“等于” 或“小于”),有关反应的离子方程式为________。用等式表示该溶液所有离子浓度间的关系________。
(4)B元素最高价氧化物晶体的硬度____(填“大”、“小”),其理由是________。
(5)C、D两元素非金属性较强的是(写元素符号)____。写出证明这一结论的一个实验事实____。
查看习题详情和答案>>
(2)写出A单质与水反应的离子化学方程式为________。
(3)A与D形成的化合物的电子式为____,溶于水后溶液的pH____7(填“大于”、“等于” 或“小于”),有关反应的离子方程式为________。用等式表示该溶液所有离子浓度间的关系________。
(4)B元素最高价氧化物晶体的硬度____(填“大”、“小”),其理由是________。
(5)C、D两元素非金属性较强的是(写元素符号)____。写出证明这一结论的一个实验事实____。
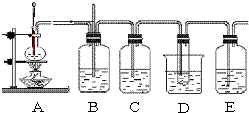 如图是制取1,2-二溴乙烷的装置,根据信息回答问题:
如图是制取1,2-二溴乙烷的装置,根据信息回答问题:1,2-二溴乙烷的主要物理性质
| 熔点 | 沸点 | 密度 | 溶解性 |
| 9.79℃ | 131.4℃ | 2.18g?cm-3 | 难溶于水,易溶于醇、醚等 |
起安全作用,当B中气体压力过大时,水就会从玻璃管上端溢出
起安全作用,当B中气体压力过大时,水就会从玻璃管上端溢出
;D装置中水的作用是冷却,减少产物的挥发
冷却,减少产物的挥发
.(2)C和E所盛都是NaOH溶液,它们的作用分别是:C
吸收乙烯中混有的SO2、CO2
吸收乙烯中混有的SO2、CO2
;E吸收逸出的溴蒸气,防止污染空气
吸收逸出的溴蒸气,防止污染空气
(3)写出以乙醇和浓硫酸制取乙烯副产物之一与溴水反应的离子方程式
SO2 +Br2 +2H2O=4H++SO42-+2Br-
SO2 +Br2 +2H2O=4H++SO42-+2Br-
.某氯化铁与氯化亚铁的混合物.现要测定其中铁元素的质量分数,实验按以下步骤进行:
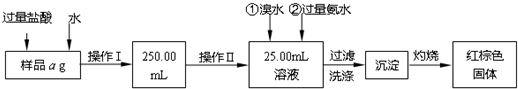
Ⅰ.请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
(2)请写出加入溴水发生的离子反应方程式
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是
若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是
×100%
×100%
Ⅱ.有同学提出,还可以采用以下方法来测定:
(1)溶解样品改用了硫酸,而不用盐酸,为什么

(2)选择的还原剂是否能用铁
(3)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是
.
查看习题详情和答案>>

Ⅰ.请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
250mL容量瓶
250mL容量瓶
、胶头滴管
胶头滴管
,(填仪器名称)(2)请写出加入溴水发生的离子反应方程式
2Fe2++Br2=2Fe3++2Br-
2Fe2++Br2=2Fe3++2Br-
,(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是
再次加热冷却并称量,直至两次质量差小于0.1g
再次加热冷却并称量,直至两次质量差小于0.1g
.若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是
| 1120(W2-W1) |
| 160a |
| 1120(W2-W1) |
| 160a |
Ⅱ.有同学提出,还可以采用以下方法来测定:
(1)溶解样品改用了硫酸,而不用盐酸,为什么
过量的盐酸对后面KMnO4的滴定有干扰
过量的盐酸对后面KMnO4的滴定有干扰

(2)选择的还原剂是否能用铁
否
否
(填“是”或“否”),原因是:如果用铁做还原剂,会与过量的硫酸反应生成Fe2+,干扰铁元素的测定
如果用铁做还原剂,会与过量的硫酸反应生成Fe2+,干扰铁元素的测定
.(3)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是
| 2.8bc |
| a |
| 2.8bc |
| a |
A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.己知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.
(1)C元素在周期表中的位置
(2)A元素与水反应的离子方程式是
(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式
(4)BD2和C2均具有漂白性,二者的漂白原理
(5)B元素的单质在不同的条件下可以与O2发生一系列反应:
B(s)+O2=BO2(g);△H=-296.8kj?mol-1
2BD2(s)+O2(g) 2BO3(g);△H=-196.6kJ?mol-1
2BO3(g);△H=-196.6kJ?mol-1
则1mol BO3(g)若完全分解成B(s),反应过程中的热效应为
(6)氢氧燃料电池能量转化率高,具有广阔的发展前景.如图(1)所示,电池中正极的电极反应式为
(7)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g) 2NGH3(g);△H=-92.4kJ/mol
2NGH3(g);△H=-92.4kJ/mol

①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图(2)所示.图中t1时引起平衡移动的条件可能是
②温度为T℃时,将2a molH2和a molN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该反应的平衡常数为
.
查看习题详情和答案>>
(1)C元素在周期表中的位置
第三周期,第VIIA族
第三周期,第VIIA族
.(2)A元素与水反应的离子方程式是
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式
Cl2+Na2S=2NaCl+S↓
Cl2+Na2S=2NaCl+S↓
.(4)BD2和C2均具有漂白性,二者的漂白原理
不同
不同
.(填“相同”或“不同”)(5)B元素的单质在不同的条件下可以与O2发生一系列反应:
B(s)+O2=BO2(g);△H=-296.8kj?mol-1
2BD2(s)+O2(g)
 2BO3(g);△H=-196.6kJ?mol-1
2BO3(g);△H=-196.6kJ?mol-1则1mol BO3(g)若完全分解成B(s),反应过程中的热效应为
△H=+395.1kJ/mol
△H=+395.1kJ/mol
.(6)氢氧燃料电池能量转化率高,具有广阔的发展前景.如图(1)所示,电池中正极的电极反应式为
O2+2H20+4e-=4OH-
O2+2H20+4e-=4OH-
.(7)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g)
 2NGH3(g);△H=-92.4kJ/mol
2NGH3(g);△H=-92.4kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图(2)所示.图中t1时引起平衡移动的条件可能是
加压
加压
.其中表示平衡混合物中NH3的含量最高的一段时间是t2-t3
t2-t3
.②温度为T℃时,将2a molH2和a molN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该反应的平衡常数为
| 4 |
| a2 |
| 4 |
| a2 |
对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的.
(1)现有下列六种物质:SO2、SiO2、CaO、MgO、Fe2O3、Na2O2.
按照不同的分类标准,它们中有一种物质与其他物质有明显的不同,请找出这种物质,并写出分类的依据.(至少要写出两种分类方法)
①
②
(2)从反应中有无离子参加,可以将化学反应分为离子反应和非离子反应,Na2O2与水反应的离子方程式是
(3)虽然分类的方法不同,但离子反应和氧化还原反应之间存在着一定的关系.请用简单的图示方法表示二者之间的关系: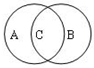
 .用离子反应方程式证明你的观点:
.用离子反应方程式证明你的观点:
查看习题详情和答案>>
(1)现有下列六种物质:SO2、SiO2、CaO、MgO、Fe2O3、Na2O2.
按照不同的分类标准,它们中有一种物质与其他物质有明显的不同,请找出这种物质,并写出分类的依据.(至少要写出两种分类方法)
①
Na2O2;
Na2O2;
;②
SO2;根据物质在常温下的状态
SO2;根据物质在常温下的状态
.(2)从反应中有无离子参加,可以将化学反应分为离子反应和非离子反应,Na2O2与水反应的离子方程式是
2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
.从反应中是否存在元素化合价的变化
是否存在元素化合价的变化
可以将化学反应分为氧化还原反应和非氧化还原反应,从上述氧化物中分别找出两种能相互反应的物质,各写一个非氧化还原反应的方程式和氧化还原反应的方程式:SiO2+CaO=CaSiO3
SiO2+CaO=CaSiO3
、SO2+Na2O2=Na2SO4
SO2+Na2O2=Na2SO4
.(3)虽然分类的方法不同,但离子反应和氧化还原反应之间存在着一定的关系.请用简单的图示方法表示二者之间的关系:


H++OH-=H2O
H++OH-=H2O
;Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
.