摘要:下列有关热化学方程式的叙述正确的是:( ) A.已知2H2(g)+O2(g) = 2H2O(g),△H=-483.6kJ/mol.则氢气的燃烧热为241.8kJ B.已知4P= P4,△H>0.则白磷比红磷稳定 C.含20.0g NaOH的稀溶液与稀硫酸完全中和.放出28.7kJ的热量.则表示该反应中和热的热化学方程式为:NaOH(aq)+1/2H2SO4(aq)= 1/2Na2SO4(aq)+H2O(l),△H=-57.4kJ/mol D.己知C(s)+ O2(g)= CO2(g),△H1C(s)+1/2 O2,△H2 则△H1>△H2
网址:http://m.1010jiajiao.com/timu3_id_312801[举报]
下列有关热化学方程式的叙述正确的是
[ ]
A、已知2H2(g)+O2(g)==2H2O(g) ΔH=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol
B、已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C、含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH+HCl=NaCl+H2O ΔH=-57.4 kJ/mol
D、已知C(s)+O2(g)==CO2(g) ΔH1 C(s)+1/2O2(g)==CO(g) ΔH2;则ΔH1<ΔH2
查看习题详情和答案>>
B、已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C、含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH+HCl=NaCl+H2O ΔH=-57.4 kJ/mol
D、已知C(s)+O2(g)==CO2(g) ΔH1 C(s)+1/2O2(g)==CO(g) ΔH2;则ΔH1<ΔH2
下列有关热化学方程式的叙述中,正确的是( )
| A、含20.0g NaOH的稀溶液与足量的稀硫酸完全中和,放出28.7kJ的热量,则表示中和热的热化学方程式为 2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-114.8kJ/mol | ||
B、已知热化学方程式:SO2(g)+
| ||
| C、已知2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol,则H2的燃烧热为241.8kJ/mol | ||
| D、已知①S(s)+O2(g)=SO2(g);△H1 ②S(g)十O2(g)=SO2(g);△H2则△H1>△H2 |
下列有关热化学方程式及其叙述正确的是( )
| A、氢气的燃烧热为285.5kJ/mo1,则水电解的热化学方程式为:2H2O(l)═2H2(g)+O2(g);△H=+285.5kJ/mol | ||||
B、1mol甲烷完全燃烧生成CO2和H2O(l)时放出890kJ热量,它的热化学方程式为
| ||||
| C、已知2C(s)+O2(g)═2CO(g);△H=-221kJ?mol-1,则C的燃烧热为110.5kJ/mol | ||||
| D、HF与NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ/mol |
下列有关叙述正确的是( )
| A、“神舟六号”返回舱表层用的是具有耐高温、抗氧化的新型无机非金属材料,高温时自动烧蚀带走热量,从而保证内部温度不致过高 | B、“含氟牙膏”、“富硒营养品”中的氟、硒指的是分子,而“高钙牛奶”和“加铁酱油”中指的是钙元素和铁元素 | C、如图为反应物A、B和生成物C的能量示意图,其反应的热化学方程式为:2 A(g)+B(g)═2 C(g)△H=Q kJ?mol-1(Q>0 )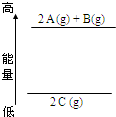 | D、实验室电解水制取氢气和氧气时通常加入硫酸钠等强电解质,目的是增强溶液的导电性 |
下列有关叙述正确的是( )
| A、稀有气体的晶体其组成微粒是原子,晶体中不存在分子间作用力 | ||
| B、金刚石的熔沸点高于晶体硅,因为C-C键能大于Si-Si键能 | ||
C、CO燃烧的热化学方程式可表示为:CO(g)+
| ||
D、C-12的原子组成符号为
|