摘要:如图所示.a曲线表示一定条件下可逆反应:X2ZΔH= -Q kJ/mol的反应过程.若使a曲线变为b曲线.可采取的措施是( ) A.加入催化剂 B.增大Y的浓度 C.降低温度 D.增大体系压强
网址:http://m.1010jiajiao.com/timu3_id_312672[举报]
如图所示,a曲线表示一定条件下可逆反应:X(g)+2Y(g) 2Z(g)+W(s) ΔH=-QkJ/mol的反应过程,若使a曲线变为b曲线,可采取的措施是
2Z(g)+W(s) ΔH=-QkJ/mol的反应过程,若使a曲线变为b曲线,可采取的措施是
 2Z(g)+W(s) ΔH=-QkJ/mol的反应过程,若使a曲线变为b曲线,可采取的措施是
2Z(g)+W(s) ΔH=-QkJ/mol的反应过程,若使a曲线变为b曲线,可采取的措施是 
[ ]
A.加入催化剂
B.增大Y的浓度
C.降低温度
D.增大体系压强
查看习题详情和答案>>
B.增大Y的浓度
C.降低温度
D.增大体系压强
如图所示,a曲线表示一定条件下可逆反应:X(g)+2Y(g)![]() 2Z(g)+W(s)
2Z(g)+W(s)
ΔH= —Q kJ/mol的反应过程,若使a曲线变为b曲线,可采取的措施是

A、加入催化剂 B、增大Y的浓度
C、降低温度 D、增大体系压强
查看习题详情和答案>>|
如图所示,a曲线表示一定条件下可逆反应:X(g)+2Y(g)
| |
| [ ] | |
A. |
加入催化剂 |
B. |
增大Y的浓度 |
C. |
降低温度 |
D. |
增大体系压强 |
一定条件下,发生如下反应:A(g)+2B(g)?xC(g)+D(g)△H<0,x为正整数).
(1)450℃时,向甲、乙两容积均为1L的恒容容器中,分别充入2molA、4molB和1molA、2molB,测得容器内c(A)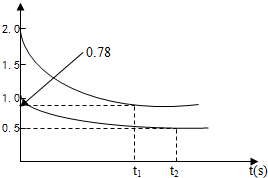 随时间变化如图所示.
随时间变化如图所示.
①x的值为
.
②甲容器内从起始到平衡时,反应速率v(B)
mol/(L?s).
③若向甲容器中再充入2molA、4molB,则达平衡时,A的物质的量浓度的范围:
(2)对(1)反应中达到平衡后的乙容器,升温至600℃时,此时K值应
(3)根据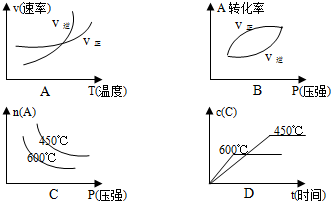 题意,下列曲线符合变化规律的是
题意,下列曲线符合变化规律的是
(4)450℃时甲容器中,判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.v (B)(正)=2v(C)(逆)
C.容器中密度不变 D.c (A)=c(D)
查看习题详情和答案>>
(1)450℃时,向甲、乙两容积均为1L的恒容容器中,分别充入2molA、4molB和1molA、2molB,测得容器内c(A)
 随时间变化如图所示.
随时间变化如图所示.①x的值为
1
1
;(以下各题均用此数据)平衡常数表达式K=| c(C)×c(D) |
| c(A)×c2(B) |
| c(C)×c(D) |
| c(A)×c2(B) |
②甲容器内从起始到平衡时,反应速率v(B)
| 2.44 |
| t1 |
| 2.44 |
| t1 |
③若向甲容器中再充入2molA、4molB,则达平衡时,A的物质的量浓度的范围:
0.78mol/L
0.78mol/L
<c(A)<1.56mol/L
1.56mol/L
.(2)对(1)反应中达到平衡后的乙容器,升温至600℃时,此时K值应
减小
减小
(填“增大”或“减小”或“不变”).(3)根据
 题意,下列曲线符合变化规律的是
题意,下列曲线符合变化规律的是ABD
ABD
.(4)450℃时甲容器中,判断该反应达到化学平衡状态的依据是
AB
AB
.A.容器中压强不变 B.v (B)(正)=2v(C)(逆)
C.容器中密度不变 D.c (A)=c(D)

