网址:http://m.1010jiajiao.com/timu3_id_312487[举报]
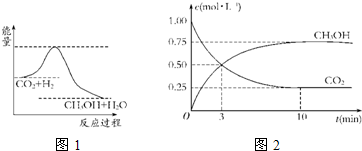
(1)关于该反应的下列说法中,正确的是
A.△H>0,△S>0; B.△H>0,△S<0;
C.△H<0,△S<0; D.△H<0,△S>0.
(2)该图中能量的最高点和最低点之间的差值代表
(3)为探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1mol CO2
和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示.从反应开始到平衡用氢气浓度变化表示的平均反应速率v(H2)
(4)肼(N2H4)是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是:
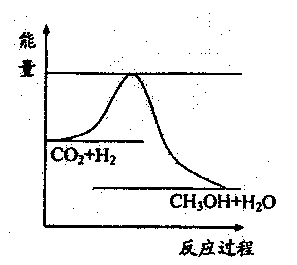 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:
 CO2(g)+3H2(g) CH3OH(g)
CO2(g)+3H2(g) CH3OH(g)
+H2O(g),右图表示该反应进行过程
中能量的变化。
(1)该反应的△H 0
(填>、<、=)。
(2)该反应平衡常数K的表达式为
。
(3)温度降低,平衡常数K (填
“增大”、‘‘不变”或“减小”)。
(4)为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入
1mol CO2 和3molH2,测得CO2和
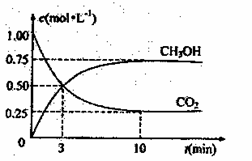 CH3OH(g)的浓度随时问变化如右图所示。
CH3OH(g)的浓度随时问变化如右图所示。
①从反应开始到平衡,用氢气浓度变化表
示的平均反应速率v(H2)=
②下列措鹧中能使n(CH3OH)/
n(CO2)增大的有 u。
A.升高温度
B.加入催化剂
C.将H20(g)从体系中分离
D.再充入l molC02和3 mol H2
E.充入He(g),使体系总压强增大
(5)甲醇、O2、KOH溶液可构成燃料电池,其负极反应式为
查看习题详情和答案>>
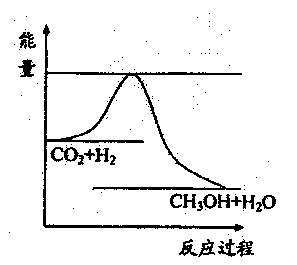 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:
 CO2(g)+3H2(g) CH3OH(g)
CO2(g)+3H2(g) CH3OH(g)
+H2O(g),右图表示该反应进行过程
中能量的变化。
(1)该反应的△H 0
(填>、<、=)。
(2)该反应平衡常数K的表达式为
。
(3)温度降低,平衡常数K (填
“增大”、‘‘不变”或“减小”)。
(4)为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入
1mol CO2 和3molH2,测得CO2和
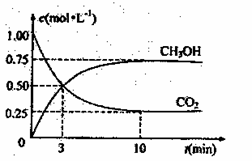 CH3OH(g)的浓度随时问变化如右图所示。
CH3OH(g)的浓度随时问变化如右图所示。
①从反应开始到平衡,用氢气浓度变化表
示的平均反应速率v(H2)=
②下列措鹧中能使n(CH3OH)/
n(CO2)增大的有 u。
A.升高温度
B.加入催化剂
C.将H20(g)从体系中分离
D.再充入l molC02和3 mol H2
E.充入He(g),使体系总压强增大
(5)甲醇、O2、KOH溶液可构成燃料电池,其负极反应式为
查看习题详情和答案>>
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
 ⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJ/mol
CH3OH(g)+H2O(g) △H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到平衡,氢气的平均反应速率v(H2)=___________mol/(L·min)。
②该反应的平衡常数表达式为__________________。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2 CO2=2 CO+O2,CO可用作燃料。
已知该反应的阳极反应为:4OH――4e―=O2↑+2H2O
则阴极反应式为:________________________________。
有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染。请你判断是否可行并说出理由:______________________________________________。
查看习题详情和答案>>(17分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验,在体积为2L的密闭容器中,充入1molCO2和3.25molH2,在一定条件下发生反应,测定CO2、CH3OH和H2O(g)的浓度随时间变化如图所示:
①写出该工业方法制取甲醇的化学方程式: 。
②从反应开始到平衡,氢气的平均反应速率v(H2)= 。
③反应到达平衡后,再向该容器中通入1 mol CO2和3.25 mol H2,重新到达平衡后,H2的转化率将 (填增大、减小或不变)
④下列措施中一定能使n(CH3OH)/ n(CO2)增大的是: 。
A.向容器中充入一定量的氦气 B.充入CO2
C.将水蒸气从体系中分离 D.用更有效的催化剂
(2)可燃性的有机物和氧气在理论上都可以作为燃料电池中的反应物,请写出CH3OH —O2—KOH燃料电池的负极的电极反应式:
(3)若将一定数量的C3H8—O2—KOH燃料电池按一定方式组成电池组以满足电解需要的电压。现用该电池组电解500mL某CuSO4的稀溶液(用铂为电极),电解后的溶液需要加入98克Cu(OH)2才能使溶液恢复到原硫酸铜溶液的浓度和质量。若忽略电池组在电解过程中的能量损失,其能量全部用来电解CuSO4溶液,则:
①原CuSO4溶液物质的量浓度
②该电池组消耗的丙烷在标准状况时的体积
查看习题详情和答案>>