摘要:下列说法正确的k*s#5^u是 ( ) A.鸡蛋白溶液中滴加饱和的k*s#5^u硫酸铵溶液.出现白色沉淀.该过程叫做蛋白质的k*s#5^u变性ks.5u B.葡萄糖.蔗糖均能与新制氢氧化铜混合加热反应生成Cu2O C.菜子油能使溴的k*s#5^u四氯化碳溶液退色 D.氨基酸具有两性.而组成多肽.蛋白质的k*s#5^u氨基酸的k*s#5^u氨基和羧基发生了缩合反应.所以多肽.蛋白质不具有两性
网址:http://m.1010jiajiao.com/timu3_id_300548[举报]
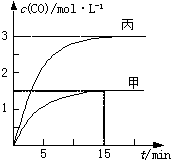 一定条件下存在反应:C(s)+H2O(g)═CO(g)+H2(g)△H>0.向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图.
一定条件下存在反应:C(s)+H2O(g)═CO(g)+H2(g)△H>0.向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图.| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | V |
| 温度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2molC 1molH2O |
1molCO 1molH2 |
4molC 2molH2O |
| A、甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol?L-1?min-1 |
| B、丙容器的体积V<0.5 L |
| C、当温度为T1℃时,反应的平衡常数K=2.25 |
| D、乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2 |
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应,在2L密闭容器中通入2mol的N2和6mol的H2,5min时反应达到平衡,此时容器内的压强变为原来的3/4,0-5min该反应的化学反应速率为V(H2)=
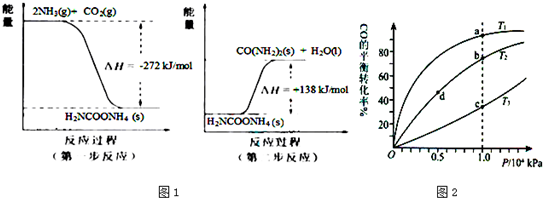
(2)NH3 (g)与CO2(g)经过两步反应生成尿素〔CO(NH2)2〕,两步反应的能量变化示意图1:
则NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为
(3)用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示.下列说法正确的是
A.温度:T1>T2>T3
B.平衡常数:K(a)>K(c)
C.平衡常数:K(b)=K(d)
D.正反应速率:v(b)>v(d)
E.平均摩尔质量:M(a)=M(c)
(4)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中C(NH+4)=C(Cl?),则溶液显(
.
查看习题详情和答案>>
(1)合成氨反应,在2L密闭容器中通入2mol的N2和6mol的H2,5min时反应达到平衡,此时容器内的压强变为原来的3/4,0-5min该反应的化学反应速率为V(H2)=
0.3mol/(L.min)
0.3mol/(L.min)
,N2的转化率=50%
50%
,化学平衡常数K=0.59
0.59
.(2)NH3 (g)与CO2(g)经过两步反应生成尿素〔CO(NH2)2〕,两步反应的能量变化示意图1:
则NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为
2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-134kJ/mol
2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-134kJ/mol
.(3)用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示.下列说法正确的是
BCD
BCD
(填字母)A.温度:T1>T2>T3
B.平衡常数:K(a)>K(c)
C.平衡常数:K(b)=K(d)
D.正反应速率:v(b)>v(d)
E.平均摩尔质量:M(a)=M(c)
(4)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中C(NH+4)=C(Cl?),则溶液显(
中
中
)性(填“酸”“碱”或“中”);用含a的代数式表示NH3?H2O的电离常数Kb=| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |

某温度下,在一个2L的密闭容器中,加入4mol A和2mol B进行如下反应:3A(g)+2B(g)?4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6mol C,则下列说法正确的是( )
已知反应①:CO(g)+CuO(s)?CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)?Cu(s)+H2O(g)在相同的温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)?CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是( )
下列说法正确的是( )
| A、Li、Na、K元素的原子核外电子层数随着核电荷数的增加而减少 | B、第二周期元素从Li到F,非金属性逐渐减弱 | C、因为K比Na容易失去电子,所以K比Na的还原性强 | D、O与S为同主族元素,且O比S的非金属性弱 |