摘要:29. 高温 (1)3CO+Fe2O3→2Fe+3CO2(2)与水和氧气同时接触,4(3)①过滤 ②取滤液少量于试管中.向试管中加入少量锌粒.有气体产生.则证明B过量 ③Fe+H2SO4→FeSO4+H2↑ Fe+ CuSO4→FeSO4+Cu
网址:http://m.1010jiajiao.com/timu3_id_30000[举报]
金属在生产和生活中应用广泛.
(1)每年因金属锈蚀造成很大浪费,铁生锈的条件是
(2)兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液.他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:
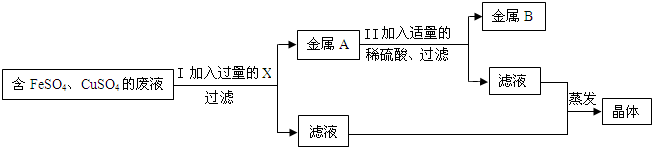
①写出Ⅰ中有关反应的化学方程式
②小红、小强同学在步骤Ⅰ中X能否改用锌的问题上产生了分歧.请你也参与他们的讨论,表明观点,并说明理由.
查看习题详情和答案>>
(1)每年因金属锈蚀造成很大浪费,铁生锈的条件是
与氧气、水同时接触
与氧气、水同时接触
;废钢铁可回收重新冶炼,高炉炼铁中一氧化碳还原氧化铁的化学方程式为3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
(2)兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液.他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:

①写出Ⅰ中有关反应的化学方程式
Fe+CuSO4 ═FeSO4 +Cu
Fe+CuSO4 ═FeSO4 +Cu
.②小红、小强同学在步骤Ⅰ中X能否改用锌的问题上产生了分歧.请你也参与他们的讨论,表明观点,并说明理由.
不能用锌;锌能够将硫酸亚铁、硫酸铜分别转化为铁、铜,生成了ZnSO4杂质
不能用锌;锌能够将硫酸亚铁、硫酸铜分别转化为铁、铜,生成了ZnSO4杂质
.(2013?昌平区一模)金属在生活和生产中有广泛的应用.
(1)下列金属制品中,利用金属导热性的是

(2)铁生锈的条件是
(3)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为
(4)工业上生产电路板及处理废液的工艺流程如下:

Ⅰ.步骤①反应的化学方程式为
Ⅱ.步骤②得到滤渣的成分是
查看习题详情和答案>>
(1)下列金属制品中,利用金属导热性的是
B
B
(填字母序号).
(2)铁生锈的条件是
与水和氧气同时接触
与水和氧气同时接触
.(3)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(4)工业上生产电路板及处理废液的工艺流程如下:

Ⅰ.步骤①反应的化学方程式为
2FeCl3+Cu=2FeCl2+CuCl2
2FeCl3+Cu=2FeCl2+CuCl2
.Ⅱ.步骤②得到滤渣的成分是
Fe和Cu
Fe和Cu
. (1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
(1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.①发热剂需接触到空气才会发热,原因是铁要与
氧气
氧气
、水
水
等物质共同作用才会生锈.防止铁制品锈蚀的方法保持铁制品表面干燥与洁净等
保持铁制品表面干燥与洁净等
.②推测发热剂成分中氯化钠的作用是
加速铁粉生锈,更快地放出热量
加速铁粉生锈,更快地放出热量
.(2)应用金属活动性顺序能帮助我们进一步学习金属性质.
已知下列各组物质间均能发生置换反应.A.Fe 和CuSO4 溶液 B.Mg和MnSO4 溶液 C.Mn和FeSO4 溶液
①写出Fe 和CuSO4 溶液反应的化学方程式
Fe+CuSO4═Cu+FeSO4
Fe+CuSO4═Cu+FeSO4
,工业上用赤铁矿炼铁的原理的化学方程式Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序
Mg、Mn、Fe、Cu
Mg、Mn、Fe、Cu
.(2013?石景山区一模)金属在生产生活中应用广泛.
(1)最初输水管材用铸铁,目前多用塑料管,输送热水一般用铜管.下列管材不属于金属材料的是

(2)钢铁生锈的条件是
(3)某同学将一小包铜粉和铁粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液.
①铜和硝酸银溶液反应的化学方程式为
②滤液中的溶质组成可能为
查看习题详情和答案>>
(1)最初输水管材用铸铁,目前多用塑料管,输送热水一般用铜管.下列管材不属于金属材料的是
C
C
(填字母序号).
(2)钢铁生锈的条件是
与氧气和水同时接触
与氧气和水同时接触
.废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
(3)某同学将一小包铜粉和铁粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液.
①铜和硝酸银溶液反应的化学方程式为
Cu+2AgNO3 ═Cu(NO3)2 +2Ag
Cu+2AgNO3 ═Cu(NO3)2 +2Ag
.②滤液中的溶质组成可能为
AgNO3、Cu(NO3)2、Fe(NO3)2或Cu(NO3)2、Fe(NO3)2 (2分)
AgNO3、Cu(NO3)2、Fe(NO3)2或Cu(NO3)2、Fe(NO3)2 (2分)
.早在春秋战国时期,我国就开始生产和使用铁器.
(1)请写出用CO和赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式
A.耐腐蚀性 B.延展性 C.导热性 D.导电性
(2)铝比铁活泼,但铝箔比铁螺丝钉耐腐蚀,铝制品耐腐蚀的原因是
(3)若要验证铜、铁、铝的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是
(4)设计从废水中回收硫酸亚铁固体和铜的实验方案如下:
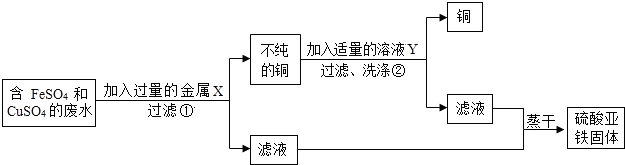
金属X是
查看习题详情和答案>>
(1)请写出用CO和赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
,盛水的铁锅与水面接触的一圈最易生锈.钢铁生锈的条件是
| ||
和氧气、水蒸气同时接触
和氧气、水蒸气同时接触
,利用新技术能将不锈钢加工成柔软的金属丝,这是利用了不锈钢的B
B
(填字母).A.耐腐蚀性 B.延展性 C.导热性 D.导电性
(2)铝比铁活泼,但铝箔比铁螺丝钉耐腐蚀,铝制品耐腐蚀的原因是
铝能和空气中的氧气反应产生一层致密的氧化膜
铝能和空气中的氧气反应产生一层致密的氧化膜
.(3)若要验证铜、铁、铝的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是
氯化铝、氯化铜或硫酸铝、硫酸铜
氯化铝、氯化铜或硫酸铝、硫酸铜
.(4)设计从废水中回收硫酸亚铁固体和铜的实验方案如下:

金属X是
铁
铁
,写出上述实验方案中有关反应的化学方程式:①Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
;②Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
.