题目内容
早在春秋战国时期,我国就开始生产和使用铁器.
(1)请写出用CO和赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式
A.耐腐蚀性 B.延展性 C.导热性 D.导电性
(2)铝比铁活泼,但铝箔比铁螺丝钉耐腐蚀,铝制品耐腐蚀的原因是
(3)若要验证铜、铁、铝的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是
(4)设计从废水中回收硫酸亚铁固体和铜的实验方案如下:
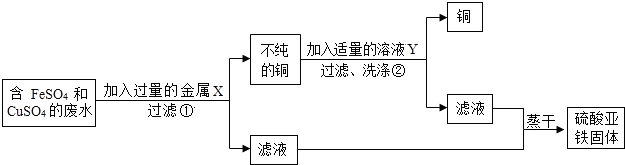
金属X是
(1)请写出用CO和赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
,盛水的铁锅与水面接触的一圈最易生锈.钢铁生锈的条件是
| ||
和氧气、水蒸气同时接触
和氧气、水蒸气同时接触
,利用新技术能将不锈钢加工成柔软的金属丝,这是利用了不锈钢的B
B
(填字母).A.耐腐蚀性 B.延展性 C.导热性 D.导电性
(2)铝比铁活泼,但铝箔比铁螺丝钉耐腐蚀,铝制品耐腐蚀的原因是
铝能和空气中的氧气反应产生一层致密的氧化膜
铝能和空气中的氧气反应产生一层致密的氧化膜
.(3)若要验证铜、铁、铝的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是
氯化铝、氯化铜或硫酸铝、硫酸铜
氯化铝、氯化铜或硫酸铝、硫酸铜
.(4)设计从废水中回收硫酸亚铁固体和铜的实验方案如下:

金属X是
铁
铁
,写出上述实验方案中有关反应的化学方程式:①Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
;②Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
.分析:(1)根据氧化铁和一氧化碳反应生成铁和二氧化碳、铁生锈的条件和不锈钢是铁的合金具有延展性分析.
(2)根据铝能和空气中的氧气反应产生一层致密的氧化铝保护膜分析.
(3)运用铁的金属活动性介于铜和铝之间所以铁能置换可溶性铜盐中的铜,不能置换可溶性铝盐中的金属铝分析.
(4)根据实验目的回收硫酸亚铁和铜、铁能和硫酸铜反应生成硫酸亚铁和铜、铁能和稀硫酸反应生成硫酸亚铁和氢气、铜不能和稀硫酸反应分析.
(2)根据铝能和空气中的氧气反应产生一层致密的氧化铝保护膜分析.
(3)运用铁的金属活动性介于铜和铝之间所以铁能置换可溶性铜盐中的铜,不能置换可溶性铝盐中的金属铝分析.
(4)根据实验目的回收硫酸亚铁和铜、铁能和硫酸铜反应生成硫酸亚铁和铜、铁能和稀硫酸反应生成硫酸亚铁和氢气、铜不能和稀硫酸反应分析.
解答:解:(1)氧化铁和一氧化碳反应生成铁和二氧化碳,铁在潮湿的空气中易生锈、不锈钢是铁的合金具有延展性所以能制成铁丝,故答案:Fe2O3+3CO
2Fe+3CO2;和氧气、水蒸气同时接触;B.
(2)铝能和空气中的氧气反应产生一层致密的氧化铝保护膜,故答案:铝能和空气中的氧气反应产生一层致密的氧化膜.
(3)铁的金属活动性介于铜和铝之间所以铁能置换可溶性铜盐中的铜,不能置换可溶性铝盐中的金属铝,故答案:氯化铝、氯化铜或硫酸铝、硫酸铜.
(4)实验目的回收硫酸亚铁和铜、铁能和硫酸铜反应生成硫酸亚铁和铜、铁能和稀硫酸反应生成硫酸亚铁和氢气、铜不能和稀硫酸反应,故答案:铁;Fe+CuSO4=FeSO4+Cu;Fe+H2SO4=FeSO4+H2↑
| ||
(2)铝能和空气中的氧气反应产生一层致密的氧化铝保护膜,故答案:铝能和空气中的氧气反应产生一层致密的氧化膜.
(3)铁的金属活动性介于铜和铝之间所以铁能置换可溶性铜盐中的铜,不能置换可溶性铝盐中的金属铝,故答案:氯化铝、氯化铜或硫酸铝、硫酸铜.
(4)实验目的回收硫酸亚铁和铜、铁能和硫酸铜反应生成硫酸亚铁和铜、铁能和稀硫酸反应生成硫酸亚铁和氢气、铜不能和稀硫酸反应,故答案:铁;Fe+CuSO4=FeSO4+Cu;Fe+H2SO4=FeSO4+H2↑
点评:充分考查了铁的冶炼、铁的锈蚀、铁的合金和铁的物理性质、铁和稀硫酸及硫酸铜两种物质的反应,综合性较强,思维角度多.

练习册系列答案
相关题目