摘要: 下列试剂可用于检验溶液中Cl-的是 A.紫色石蕊溶液 B.硝酸银溶液和稀硝酸 C.澄清石灰水 D.硝酸钡溶液和稀硝酸 22. 乙烯与溴的四氯化碳溶液可发生反应:CH2==CH2+Br2 CH2Br-CH2Br.该反应属于 A.取代反应 B.消去反应 C.加成反应 D.聚合反应
网址:http://m.1010jiajiao.com/timu3_id_295970[举报]
铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响,请完成下列各题.
在化学反应中,铜元素可表示为0、+1、+2价.
①在西汉古藉中.曾有记载:曾青得铁则化为铜[即:曾青(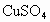 )跟铁反应就生成铜].试写出该反应的化学方程式:________________.
)跟铁反应就生成铜].试写出该反应的化学方程式:________________.
②铜器表面有时会生成铜绿[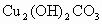 ]__________________,这层铜绿可用化学方法除去.试写出除去铜绿而不损伤器物的反应的化学方程式__________________.
]__________________,这层铜绿可用化学方法除去.试写出除去铜绿而不损伤器物的反应的化学方程式__________________.
③新制的铜试剂[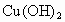 ]与葡萄糖反应生成红色沉淀,因此该试剂可用于检验糖尿病人尿液中的葡萄糖的含量,葡萄糖的结构
]与葡萄糖反应生成红色沉淀,因此该试剂可用于检验糖尿病人尿液中的葡萄糖的含量,葡萄糖的结构
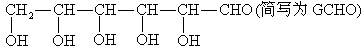
试写出葡萄糖与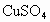 反应的化学方程式:____________________.
反应的化学方程式:____________________.
铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响,请完成下列各题.
在化学反应中,铜元素可表示为0、+1、+2价.
①在西汉古藉中.曾有记载:曾青得铁则化为铜[即:曾青(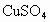 )跟铁反应就生成铜].试写出该反应的化学方程式:________________.
)跟铁反应就生成铜].试写出该反应的化学方程式:________________.
②铜器表面有时会生成铜绿[ ]__________________,这层铜绿可用化学方法除去.试写出除去铜绿而不损伤器物的反应的化学方程式__________________.
]__________________,这层铜绿可用化学方法除去.试写出除去铜绿而不损伤器物的反应的化学方程式__________________.
③新制的铜试剂[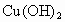 ]与葡萄糖反应生成红色沉淀,因此该试剂可用于检验糖尿病人尿液中的葡萄糖的含量,葡萄糖的结构
]与葡萄糖反应生成红色沉淀,因此该试剂可用于检验糖尿病人尿液中的葡萄糖的含量,葡萄糖的结构
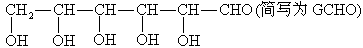
试写出葡萄糖与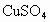 反应的化学方程式:____________________.
反应的化学方程式:____________________.
 已知:CH3CH2OH+NaBr+H2SO4(浓)
已知:CH3CH2OH+NaBr+H2SO4(浓)| △ |
实验室制备溴乙烷(沸点为38.4℃)的装置和步骤如下:
①按如图所示连接仪器,检查装置的气密性,然后向U形管和大烧杯里加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小火加热,使其充分反应.
试回答下列问题:
(1)反应时若温度过高可看到有红棕色气体产生,该气体的化学式为
Br2
Br2
.(2)反应结束后,U形管中粗制的溴乙烷呈棕黄色.将U形管中的混合物倒入分液漏斗中,静置,待液体分层后,分液,取
下层
下层
(填“上层”或“下层”)液体.为了除去其中的杂质,可选择下列试剂中的AC
AC
(填序号).A.Na2SO3溶液 B.H2O C.Na2CO3溶液 D.CCl4
(3)要进一步制得纯净的C2H5Br,可再用水洗,然后加入无水CaCl2干燥,再进行
蒸馏
蒸馏
(填操作名称).(4)下列几项实验步骤,可用于检验溴乙烷中的溴元素,其正确的操作顺序是:取少量溴乙烷,然后
④①⑤③②
④①⑤③②
(填序号).①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液 ⑤冷却
请写出在此过程中,有溴乙烷参加的主要反应的化学方程式
CH3CH2Br+NaOH
CH3CH2OH+NaBr
| △ |
CH3CH2Br+NaOH
CH3CH2OH+NaBr
.| △ |
(2012?淄博一模)铁黄是一种重要的颜料,化学式为Fe2O3?xH2O,广泛用于涂料、橡胶、塑料、文教用品等工业.实验室模拟工业利用硫酸渣(含Fe2O3及少量的CaO、MgO等)和黄铁矿粉(主要成分为FeS2)制备铁黄的流程如图:
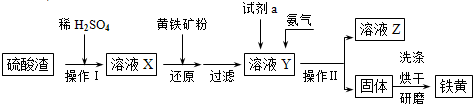
(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是
(2)试剂a最好选用
(3)上述步骤中需用到氨气.下列装置可用于实验室制氨气的是
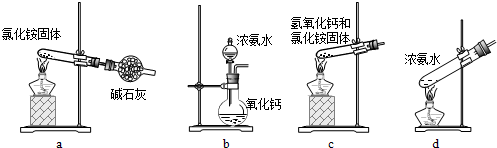
(4)检验溶液Z中含有N
的方法是
(5)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示.
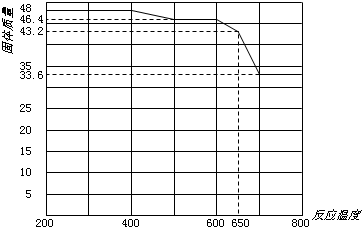
根据图象推断670℃时Fe2O3还原产物的化学式为
查看习题详情和答案>>

(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是
搅拌加速溶解(或搅拌加速反应)
搅拌加速溶解(或搅拌加速反应)
、引流
引流
.(2)试剂a最好选用
空气
空气
(供选择使用的有:铝粉、空气、浓HNO3);其作用是作氧化剂,将Fe2+氧化为Fe3+
作氧化剂,将Fe2+氧化为Fe3+
.(3)上述步骤中需用到氨气.下列装置可用于实验室制氨气的是
bd
bd
(填序号).
(4)检验溶液Z中含有N
| H | + 4 |
取少量溶液Z置于试管中,滴加过量浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝色,证明含有NH4+
取少量溶液Z置于试管中,滴加过量浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝色,证明含有NH4+
.(5)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示.

根据图象推断670℃时Fe2O3还原产物的化学式为
FeO
FeO
,并设计一个简单的实验,证明该还原产物的成分(简述实验操作、现象和结论).取少量还原产物置于试管中,加入过量稀硫酸(或稀盐酸),固体完全溶解且无气泡产生;再向其中滴加KSCN溶液,溶液不变色;最后滴加H2O2溶液,溶液变红色,证明还原产物为FeO.
取少量还原产物置于试管中,加入过量稀硫酸(或稀盐酸),固体完全溶解且无气泡产生;再向其中滴加KSCN溶液,溶液不变色;最后滴加H2O2溶液,溶液变红色,证明还原产物为FeO.
.仪器自选.可供选择的试剂:稀H2SO4、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液.(2010?西城区模拟)有机物A是合成解热镇痛药阿司匹林( )和治疗溃疡药奥沙拉嗪钠(C14H8O6N2Na2)的原料
)和治疗溃疡药奥沙拉嗪钠(C14H8O6N2Na2)的原料 .
.
(1)实验室用A和乙酸酐[化学式为(CH3CO)2O]反应合成阿司匹林.
①由A合成阿司匹林反应的化学方程式是
 .
.
②反应结束时,可用于检验A是否转化完全的试剂是
(2)由A合成奥沙拉嗪钠的路线如图所示:
①C含有的官能团名称是
②D可能发生反应的反应类型是
a.取代反应;b.加成反应;c.消去反应;d.氧化反应
③E的分子结构对称,其核磁共振氢谱具有5个吸收峰,则奥沙拉嗪钠的结构简式是
 .
.
④符合下列条件的B的同分异构体J有
a.J分子内苯环上有2个取代基,且能发生水解反应和银镜反应;b.1mol J与足量的Na反应生成0.5mol H2.
查看习题详情和答案>>
 )和治疗溃疡药奥沙拉嗪钠(C14H8O6N2Na2)的原料
)和治疗溃疡药奥沙拉嗪钠(C14H8O6N2Na2)的原料 .
.(1)实验室用A和乙酸酐[化学式为(CH3CO)2O]反应合成阿司匹林.
①由A合成阿司匹林反应的化学方程式是


②反应结束时,可用于检验A是否转化完全的试剂是
饱和溴水或FeCl3溶液
饱和溴水或FeCl3溶液
;可用于检测产物阿司匹林含有的官能团的物理方法是测其红外光谱
测其红外光谱
.(2)由A合成奥沙拉嗪钠的路线如图所示:
①C含有的官能团名称是
羟基、酯基和硝基
羟基、酯基和硝基
.②D可能发生反应的反应类型是
abd
abd
.a.取代反应;b.加成反应;c.消去反应;d.氧化反应
③E的分子结构对称,其核磁共振氢谱具有5个吸收峰,则奥沙拉嗪钠的结构简式是


④符合下列条件的B的同分异构体J有
6
6
种.a.J分子内苯环上有2个取代基,且能发生水解反应和银镜反应;b.1mol J与足量的Na反应生成0.5mol H2.