摘要:3.下列有关离子反应的叙述不正确的是 A.溶液中有难溶于水的沉淀生成是离子反应的发生条件之一 B.离子反应发生的方向总是向着溶液中离子浓度降低的方向进行 C.离子反应生成的沉淀的溶解度为零 D.生成沉淀的离子反应之所以能发生.在于生成物的溶解度小
网址:http://m.1010jiajiao.com/timu3_id_294564[举报]
有关下列装置的叙述不正确的是

| A.图①铝片发生的电极反应式是:Al+4OH--3e-===AlO2-+2H2O |
| B.图②发生析氢腐蚀,离子反应方程式为:Fe+2H+===Fe2++H2↑ |
| C.图③溶液中发生了变化:4Fe(OH)2+O2+2H2O===4Fe(OH)3 |
| D.图④充电时,阳极反应是:PbSO4+2H2O-2e-===PbO2+SO42-+4H+ |
有关下列装置的叙述不正确的是
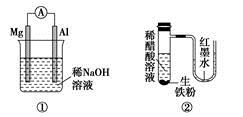


| A.图①铝片发生的电极反应式是:Al+4OH--3e-===AlO2-+2H2O |
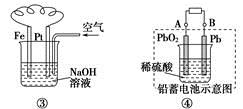
| B.图②发生析氢腐蚀,离子反应方程式为:Fe+2H+===Fe2++H2↑ |
| C.图③溶液中发生了变化:4Fe(OH)2+O2+2H2O===4Fe(OH)3 |
| D.图④充电时,阳极反应是:PbSO4+2H2O-2e-===PbO2+SO42-+4H+ |
有关下列装置的叙述不正确的是( )
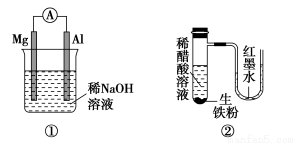
A.图①铝片发生的电极反应式是:Al+4OH--3e-=AlO2—+2H2O
B.图②发生析氢腐蚀,离子反应方程式为:Fe+2H+=Fe2++H2↑
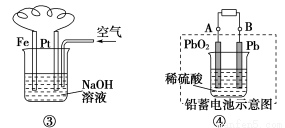
C.图③溶液中发生了变化:4Fe(OH)2+O2+2H2O=4Fe(OH)3
D.图④充电时,阳极反应是:PbSO4+2H2O-2e-=PbO2+SO42—+4H+
查看习题详情和答案>>
有关下列装置的叙述不正确的是( )

| A.图①铝片发生的电极反应式是:Al+4OH--3e-=AlO2—+2H2O |
| B.图②发生析氢腐蚀,离子反应方程式为:Fe+2H+=Fe2++H2↑ |
| C.图③溶液中发生了变化:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.图④充电时,阳极反应是:PbSO4+2H2O-2e-=PbO2+SO42—+4H+ |
 ;
;