摘要:答案:1个单位的正电荷 1个单位的负电荷 相等 相反核外电子数 质子数 质子数
网址:http://m.1010jiajiao.com/timu3_id_29316[举报]
化学用语是学习化学的基础.
(1)分别用化学式及化学符号表示:
①硫酸根离子
Cl2
Cl2.
(2)写出下列符号中“2”的含义:
①H2
(3)写出下列反应的化学方程式:(有多个答案的只需写出一种即可)
①硫在氧气中燃烧
②有水生成的化学反应
查看习题详情和答案>>
(1)分别用化学式及化学符号表示:
①硫酸根离子
SO42-
SO42-
;②硝酸银AgNO3
AgNO3
;③氯化钙中钙元素显+2价| +2 |
| Ca |
| +2 |
| Ca |
(2)写出下列符号中“2”的含义:
①H2
一个氢分子含有2个氢原子
一个氢分子含有2个氢原子
;②Cu2+一个铜离子带两个单位的正电荷
一个铜离子带两个单位的正电荷
③;2N2个氮原子
2个氮原子
.(3)写出下列反应的化学方程式:(有多个答案的只需写出一种即可)
①硫在氧气中燃烧
S+O2
SO2
| ||
S+O2
SO2
;
| ||
②有水生成的化学反应
2H2+O2
2H2O
| ||
2H2+O2
2H2O
.
| ||
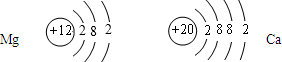 (2006?白下区二模)元素周期表中,钙元素和镁元素同在一个纵行里,它们的原子结构示意图如图所示,则:
(2006?白下区二模)元素周期表中,钙元素和镁元素同在一个纵行里,它们的原子结构示意图如图所示,则:(1)钙与镁的化学性质
相似
相似
(填“相似”、“相同”或“不同“),理由是其最外层电子数相同
其最外层电子数相同
.(2)钙元素的核电荷数为
20
20
;在元素周期表中属第4
4
周期;钙离子的化学符号为Ca2+
Ca2+
;钙离子与镁原子的不同在于钙离子带两个单位正电荷,而镁原子不带电(其他合理答案均可)
钙离子带两个单位正电荷,而镁原子不带电(其他合理答案均可)
.(1)填写下列表格:
(2)用下列物质的序号回答有关问题:(注意有的空格不只有一个答案,多填、少填均不给分)
①雨水 ②蒸馏水 ③雨后洁净的空气 ④四氧化三铁 ⑤液氮 ⑥高锰酸钾完全分解后的固体产物
其中属于混合物是
查看习题详情和答案>>
| 化学符号 | 名称或意义(只写一种) | ||||
| (1) | H | ① 氢元素 氢元素 | |||
| 2P2O5 | ② 两个五氧化二磷分子 两个五氧化二磷分子 | ||||
| Al3+ | ③ 一个铝离子带三个单位的正电荷 一个铝离子带三个单位的正电荷 | ||||
| (2) | ④ 2Ca 2Ca |
2个钙原子 | |||
| ⑤ O3 O3 |
由3个氧原子构成的一个臭氧分子 | ||||
⑥
|
氯化亚铁中铁元素显+2价 |
①雨水 ②蒸馏水 ③雨后洁净的空气 ④四氧化三铁 ⑤液氮 ⑥高锰酸钾完全分解后的固体产物
其中属于混合物是
①③⑥
①③⑥
,属于纯净物是②④⑤
②④⑤
,属于单质的是⑤
⑤
,属于氧化物的是②④
②④
.构建科学的物质“微粒观”于初中化学学习非常重要.
(1)如图1是电解水微观示意图:
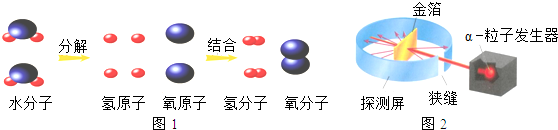
上述微观图示可以得出有关原子、分子或从分子、原子角度认识化学反应的相关结论是
(2)A、B、C、D表示四种物质,其微观示意图见下表.A和B在一定条件下反应生成C和D.
①上述物质中属于氧化物的是:
②A物质中两元素的质量比为
(3)英籍新西兰物理学家进行了如图2所示的用α-粒子轰击金箔的实验,创建了新的原子模型学说,于认识原子结构具有重要的意义.其实验现象为:大 部分α-粒子不改变原运动方向穿过金箔;一小部分α-粒 子改变了原运动路径发生了偏转;极少数α-粒子被反弹回来.根据上述实验现象可能得到的有关原子结构的结论是:
友情提示:每个α粒子带两个单位的正电荷;α粒子的质量是金原子质量的
,是电子质量的7000倍.
查看习题详情和答案>>
(1)如图1是电解水微观示意图:

上述微观图示可以得出有关原子、分子或从分子、原子角度认识化学反应的相关结论是
分子由原子构成;化学变化中原子种类、数目不变;化学变化中分子可以再分而原子不能再分.(其它答案合理也可)
分子由原子构成;化学变化中原子种类、数目不变;化学变化中分子可以再分而原子不能再分.(其它答案合理也可)
.| 物质 | A | B | C | D |  --氢原子 --氢原子 --氧原子 --氧原子 --硫原子 --硫原子 |
| 微观示意图 |  |
 |
 |
 |
①上述物质中属于氧化物的是:
D
D
;[填序号]②A物质中两元素的质量比为
1:16
1:16
;D物质中氢元素的质量分数为11.1%
11.1%
.(3)英籍新西兰物理学家进行了如图2所示的用α-粒子轰击金箔的实验,创建了新的原子模型学说,于认识原子结构具有重要的意义.其实验现象为:大 部分α-粒子不改变原运动方向穿过金箔;一小部分α-粒 子改变了原运动路径发生了偏转;极少数α-粒子被反弹回来.根据上述实验现象可能得到的有关原子结构的结论是:
原子核很小
原子核很小
,得出该结论依据的实验现象是大多数α粒子能穿透金箔,而且不改变原来的前进方向
大多数α粒子能穿透金箔,而且不改变原来的前进方向
.友情提示:每个α粒子带两个单位的正电荷;α粒子的质量是金原子质量的
| 1 |
| 49 |