题目内容
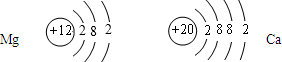 (2006?白下区二模)元素周期表中,钙元素和镁元素同在一个纵行里,它们的原子结构示意图如图所示,则:
(2006?白下区二模)元素周期表中,钙元素和镁元素同在一个纵行里,它们的原子结构示意图如图所示,则:(1)钙与镁的化学性质
相似
相似
(填“相似”、“相同”或“不同“),理由是其最外层电子数相同
其最外层电子数相同
.(2)钙元素的核电荷数为
20
20
;在元素周期表中属第4
4
周期;钙离子的化学符号为Ca2+
Ca2+
;钙离子与镁原子的不同在于钙离子带两个单位正电荷,而镁原子不带电(其他合理答案均可)
钙离子带两个单位正电荷,而镁原子不带电(其他合理答案均可)
.分析:(1)元素的化学性质由原子的最外层电子数决定,同一个纵行的元素的原子最外层电子数相同,所以化学性质相似.据此分析判断即可.
(2)依据原子结构示意图的意义以及元素周期表的特点和原子得失电子的规律分析解答即可;
(2)依据原子结构示意图的意义以及元素周期表的特点和原子得失电子的规律分析解答即可;
解答:解:(1)决定元素化学性质的是最外层电子数;元素周期表中,钙元素和镁元素同在一个纵行里,由原子结构示意图可知,钙与镁原子的最外层电子数相同,故它们的化学性质相似.
(2)由钙原子的结构示意图可知钙元素的核电荷数为20,电子层数是4,所以属于第四周期,其最外层电子数是2,化学反应中易失掉这两个电子,所以其离子符号为Ca2+;钙离子与镁原子的不同可通过是否带电等方面分析;
故答案为:(1)相似;它们的最外电子层相同.(2)20;4;Ca2+;钙离子带两个单位正电荷,而镁原子不带电;(其他合理答案均可)
(2)由钙原子的结构示意图可知钙元素的核电荷数为20,电子层数是4,所以属于第四周期,其最外层电子数是2,化学反应中易失掉这两个电子,所以其离子符号为Ca2+;钙离子与镁原子的不同可通过是否带电等方面分析;
故答案为:(1)相似;它们的最外电子层相同.(2)20;4;Ca2+;钙离子带两个单位正电荷,而镁原子不带电;(其他合理答案均可)
点评:本题难度不大,掌握决定元素化学性质的是最外层电子数以及原子结构示意图的意义即可正确解题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
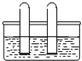 (2006?白下区二模)利用如图装置,水槽中分别盛放水、酸、碱,都无法区别的一组气体是( )
(2006?白下区二模)利用如图装置,水槽中分别盛放水、酸、碱,都无法区别的一组气体是( )