摘要:14.已知. 则反应 的△H为 A. B. C. D.
网址:http://m.1010jiajiao.com/timu3_id_291805[举报]
|
已知,H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ·mol-1则反应HCl(g)=1/2H2(g)+1/2Cl2(g)的ΔH为 | |
| [ ] | |
A. |
+184.6 kJ·mol-1 |
B. |
-92.3 kJ·mol-1 |
C. |
-36.92 kJ·mol-1 |
D. |
+92.3 kJ·mol-1 |
已知某些化学键键能的数据如表所示
(1)下列物质最不稳定的是
A.HCl B.HBr C.HI
(2)氢气与氯气反应生成氯化氢气体的热化学方程式为:
该反应是
相同条件下,1molCl2和1molH2的总能量
(3)I2(g)+H2(g)=2HI(g)△H1
I2(s)+H2(g)=2HI(g)△H2
I2(s)=I2(g)△H3
则△H1△H2△H3之间的关系为:△H1=
(4)H2和O2反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式
(可能用上的相对原子质量:H 1O 16)
查看习题详情和答案>>
| 化学键 | Cl-Cl | Br-Br | I-I | H-Cl | H-Br | H-I | H-H |
| 键能(kJ/mol) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
C
C
A.HCl B.HBr C.HI
(2)氢气与氯气反应生成氯化氢气体的热化学方程式为:
H2(g)+Cl2(g)=2HCl(g)△H=-185kJ/mol
H2(g)+Cl2(g)=2HCl(g)△H=-185kJ/mol
,该反应是
放热反应
放热反应
(选填“吸热反应”或“放热反应”).相同条件下,1molCl2和1molH2的总能量
大于
大于
2molHCl的总能量(选填:大于、小于或等于)(3)I2(g)+H2(g)=2HI(g)△H1
I2(s)+H2(g)=2HI(g)△H2
I2(s)=I2(g)△H3
则△H1△H2△H3之间的关系为:△H1=
△H2-△H3
△H2-△H3
(用△H2△H3代数式表示)(4)H2和O2反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式
H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol
| 1 |
| 2 |
H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol
.若1g水蒸气转化成液态水时放热a kJ热量,则反应 H2(g)+1/2O2(g)═H2O(l) 的△H=| 1 |
| 2 |
-(241.8+18a)kJ/mol
-(241.8+18a)kJ/mol
;4g H2完全燃烧生成水蒸气时放出的热量为:483.6kJ
483.6kJ
(可能用上的相对原子质量:H 1O 16)
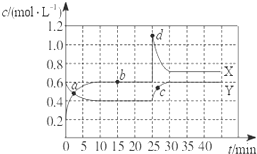 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是( )
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是( )