网址:http://m.1010jiajiao.com/timu3_id_290427[举报]
①既属于分解反应,又属于氧化还原反应的是
②属于分解反应,但不属于氧化还原反应的是
③既属于化合反应,又属于氧化还原反应的是
④属于化合反应,但不属于氧化还原反应的是
⑤不属于四种基本反应类型的氧化还原反应的是
A.(NH4)2SO3
| ||
B.2CO+O2
| ||
C.2C+SiO2
| ||
D.NH4NO3
| ||
E.CaCO3+CO2+H2O=Ca(HCO3)2
F.MnO2+4HCl(浓)
| ||
Ⅱ.(1)在一定条件下可以进行如下反应:8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为
(2)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气.
①用单线桥表示出该反应的电子转移情况:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂
Ⅰ.请把符合要求的化学方程式的字母填在下列空白处:
①既属于分解反应,又属于氧化还原反应的是______.
②属于分解反应,但不属于氧化还原反应的是______.
③既属于化合反应,又属于氧化还原反应的是______.
④属于化合反应,但不属于氧化还原反应的是______.
⑤不属于四种基本反应类型的氧化还原反应的是______.
A.(NH4)2SO3 2NH3↑+H2O+SO2↑
2NH3↑+H2O+SO2↑
B.2CO+O2 2CO2
2CO2
C.2C+SiO2 Si+2CO↑
Si+2CO↑
D.NH4NO3 N2O+2H2O
N2O+2H2O
E.CaCO3+CO2+H2O=Ca(HCO3)2
F.MnO2+4HCl(浓) MnCl2+H2O+Cl2↑
MnCl2+H2O+Cl2↑
Ⅱ.(1)在一定条件下可以进行如下反应:8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为______.
(2)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气.
①用单线桥表示出该反应的电子转移情况:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂______mol,被氧化的物质的质量为______ g.
查看习题详情和答案>>
①既属于分解反应,又属于氧化还原反应的是______.
②属于分解反应,但不属于氧化还原反应的是______.
③既属于化合反应,又属于氧化还原反应的是______.
④属于化合反应,但不属于氧化还原反应的是______.
⑤不属于四种基本反应类型的氧化还原反应的是______.
A.(NH4)2SO3
| ||
B.2CO+O2
| ||
C.2C+SiO2
| ||
D.NH4NO3
| ||
E.CaCO3+CO2+H2O=Ca(HCO3)2
F.MnO2+4HCl(浓)
| ||
Ⅱ.(1)在一定条件下可以进行如下反应:8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为______.
(2)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气.
①用单线桥表示出该反应的电子转移情况:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂______mol,被氧化的物质的质量为______ g.
①既属于分解反应,又属于氧化还原反应的是______.
②属于分解反应,但不属于氧化还原反应的是______.
③既属于化合反应,又属于氧化还原反应的是______.
④属于化合反应,但不属于氧化还原反应的是______.
⑤不属于四种基本反应类型的氧化还原反应的是______.
A.(NH4)2SO3
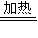 2NH3↑+H2O+SO2↑
2NH3↑+H2O+SO2↑B.2CO+O2
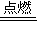 2CO2
2CO2C.2C+SiO2
 Si+2CO↑
Si+2CO↑D.NH4NO3
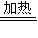 N2O+2H2O
N2O+2H2OE.CaCO3+CO2+H2O=Ca(HCO3)2
F.MnO2+4HCl(浓)
 MnCl2+H2O+Cl2↑
MnCl2+H2O+Cl2↑Ⅱ.(1)在一定条件下可以进行如下反应:8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为______.
(2)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气.
①用单线桥表示出该反应的电子转移情况:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂______mol,被氧化的物质的质量为______ g.
查看习题详情和答案>>
(12分)
A.下图是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:
|
| |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ⑨ | |||||||||||||||
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,①元素位于周期表
的 区。
(2)②、⑥两元素形成的化合物的空间构型为 ,其中心原子的杂化类型为 。
(3)写出元素⑧基态原子的电子排布式 。
(4)①③两元素形成的最简单的化合物与 (写微粒符号)互为等电子体。
(5)元素⑦与CO可形成的X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于___ 晶体(填晶体类型)。
(6)元素⑨的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力
为 。
(7) 金属⑦的晶体在不同温度下有两种堆积方式,晶胞分 别如右图所示。 则面心立方晶胞和体心立方晶胞中实际含有的原子个数之比为 。
则面心立方晶胞和体心立方晶胞中实际含有的原子个数之比为 。
B.(12分)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇
2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(g)①,25℃时, K=2.95×1011
CH3CH2OH(g)+3H2O(g)①,25℃时, K=2.95×1011
2CO(g)+4H2(g) ![]() CH3CH2OH(g)+H2O(g)②,25℃时, K=1.71×1022
CH3CH2OH(g)+H2O(g)②,25℃时, K=1.71×1022
(1)写出反应①的平衡常数表达式K=__________________。
(2)条件相同时,反应①与反应②相比,转化程度更大的是________。以CO2为原料合成乙醇的优点是 (写出一条即可)。
 |
(3)在一定压强下,测得反应①的实验数据如下表:
根据表中数据分析:
①温度升高,K值______(填“增大”、“减小”或“不变”)。
②提高氢碳比[ n(H2)/n(CO2)],对生成乙醇 (填“有利”、“不利”)。
 (4)在下图的坐标中作图说明压强变化对反应①的化学平衡的影响。(必须在图中标明坐标轴所表示的物理量。
(4)在下图的坐标中作图说明压强变化对反应①的化学平衡的影响。(必须在图中标明坐标轴所表示的物理量。
 ①
①