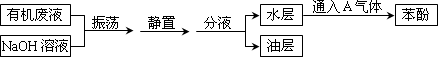
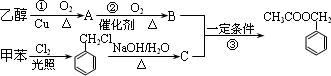
题目内容
Ⅰ.请把符合要求的化学方程式的字母填在下列空白处:
①既属于分解反应,又属于氧化还原反应的是______.
②属于分解反应,但不属于氧化还原反应的是______.
③既属于化合反应,又属于氧化还原反应的是______.
④属于化合反应,但不属于氧化还原反应的是______.
⑤不属于四种基本反应类型的氧化还原反应的是______.
A.(NH4)2SO3 2NH3↑+H2O+SO2↑
2NH3↑+H2O+SO2↑
B.2CO+O2 2CO2
2CO2
C.2C+SiO2 Si+2CO↑
Si+2CO↑
D.NH4NO3 N2O+2H2O
N2O+2H2O
E.CaCO3+CO2+H2O=Ca(HCO3)2
F.MnO2+4HCl(浓) MnCl2+H2O+Cl2↑
MnCl2+H2O+Cl2↑
Ⅱ.(1)在一定条件下可以进行如下反应:8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为______.
(2)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气.
①用单线桥表示出该反应的电子转移情况:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂______mol,被氧化的物质的质量为______ g.
解:Ⅰ、A、(NH4)2SO3 2NH3↑+H2O+SO2↑,属于分解反应,不是氧化还原反应;
2NH3↑+H2O+SO2↑,属于分解反应,不是氧化还原反应;
B.2CO+O2 2CO2;反应属于化合反应,是氧化还原反应;
2CO2;反应属于化合反应,是氧化还原反应;
C.2C+SiO2 Si+2CO↑;反应是置换反应,属于氧化还原反应;
Si+2CO↑;反应是置换反应,属于氧化还原反应;
D.NH4NO3 N2O+2H2O;反应是分解反应,是氧化还原反应;
N2O+2H2O;反应是分解反应,是氧化还原反应;
E.CaCO3+CO2+H2O=Ca(HCO3)2 ;反应是化合反应,不是氧化还原反应;
F.MnO2+4HCl(浓) MnCl2+H2O+Cl2↑;反应是氧化还原反应;
MnCl2+H2O+Cl2↑;反应是氧化还原反应;
故答案为:Ⅰ.①D ②A ③B ④E ⑤F
Ⅱ.(1)依据氧化还原反应的电子守恒计算,根据化合价升降分析,8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,该反应中氧化剂与还原剂的物质的量之比为5:2,标注化合价求化合价升降判断氧化剂还原剂,还原剂:2Mn2+~2MnO4-~10e-;氧化剂:5R2O8n-~10RO42-~(20-5n)e-,依据电子守恒得到:10=20-5n,n=2,故答案为:2;
(2)①用单线桥表示出该反应的电子转移情况为: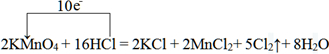
故答案为: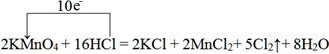 ;
;
②反应为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;在标准状况下,该反应产生2.24L Cl2时物质的量为0.1mol,氧化剂为KMnO4,2KMnO4~5Cl2,消耗氧化剂KMnO4为0.04mol;被氧化的物质为HCl,氧化剂和还原剂的定量关系为:2KMnO4~10HCl,所以被氧化的氯化氢物质的量为0.2mol,氯化氢的质量=0.2mol×36.5g/mol=7.3g;
故答案为:0.04;7.3.
分析:Ⅰ,①依据概念分析判断,分解反应是一种物质生成两种或两种以上物质的反应,氧化还原反应是反应前后存在元素化合价的变化;
②依据概念分析判断,分解反应是一种物质生成两种或两种以上物质的反应,氧化还原反应是反应前后存在元素化合价的变化;
③据概念分析判断,化合反应是两种或两种以上物质的反应生成一种物质的反应,氧化还原反应是反应前后存在元素化合价的变化;
④据概念分析判断,化合反应是两种或两种以上物质的反应生成一种物质的反应,氧化还原反应是反应前后存在元素化合价的变化;
⑤四种基本反应类型为化合反应、分解反应、置换反应、复分解反应;氧化还原反应是反应前后存在元素化合价的变化;
Ⅱ、(1)依据反应前后电子守恒分析计算;
(2)①单线桥表示出该反应的电子转移,是标明电子转移方向和数目;
②依据化学方程式,结合氧化还原反应的概念进行计算;
点评:本题考查了化学反应类型的分析判断,氧化还原反应的概念判断,化学方程式的书写,氧化还原反应的电子转移计算和单线桥表示,电子守恒是氧化还原反应常用计算依据.
 2NH3↑+H2O+SO2↑,属于分解反应,不是氧化还原反应;
2NH3↑+H2O+SO2↑,属于分解反应,不是氧化还原反应;B.2CO+O2
 2CO2;反应属于化合反应,是氧化还原反应;
2CO2;反应属于化合反应,是氧化还原反应;C.2C+SiO2
 Si+2CO↑;反应是置换反应,属于氧化还原反应;
Si+2CO↑;反应是置换反应,属于氧化还原反应;D.NH4NO3
 N2O+2H2O;反应是分解反应,是氧化还原反应;
N2O+2H2O;反应是分解反应,是氧化还原反应;E.CaCO3+CO2+H2O=Ca(HCO3)2 ;反应是化合反应,不是氧化还原反应;
F.MnO2+4HCl(浓)
 MnCl2+H2O+Cl2↑;反应是氧化还原反应;
MnCl2+H2O+Cl2↑;反应是氧化还原反应;故答案为:Ⅰ.①D ②A ③B ④E ⑤F
Ⅱ.(1)依据氧化还原反应的电子守恒计算,根据化合价升降分析,8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,该反应中氧化剂与还原剂的物质的量之比为5:2,标注化合价求化合价升降判断氧化剂还原剂,还原剂:2Mn2+~2MnO4-~10e-;氧化剂:5R2O8n-~10RO42-~(20-5n)e-,依据电子守恒得到:10=20-5n,n=2,故答案为:2;
(2)①用单线桥表示出该反应的电子转移情况为:
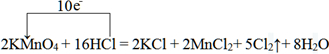
故答案为:
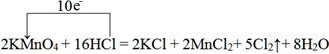 ;
;②反应为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;在标准状况下,该反应产生2.24L Cl2时物质的量为0.1mol,氧化剂为KMnO4,2KMnO4~5Cl2,消耗氧化剂KMnO4为0.04mol;被氧化的物质为HCl,氧化剂和还原剂的定量关系为:2KMnO4~10HCl,所以被氧化的氯化氢物质的量为0.2mol,氯化氢的质量=0.2mol×36.5g/mol=7.3g;
故答案为:0.04;7.3.
分析:Ⅰ,①依据概念分析判断,分解反应是一种物质生成两种或两种以上物质的反应,氧化还原反应是反应前后存在元素化合价的变化;
②依据概念分析判断,分解反应是一种物质生成两种或两种以上物质的反应,氧化还原反应是反应前后存在元素化合价的变化;
③据概念分析判断,化合反应是两种或两种以上物质的反应生成一种物质的反应,氧化还原反应是反应前后存在元素化合价的变化;
④据概念分析判断,化合反应是两种或两种以上物质的反应生成一种物质的反应,氧化还原反应是反应前后存在元素化合价的变化;
⑤四种基本反应类型为化合反应、分解反应、置换反应、复分解反应;氧化还原反应是反应前后存在元素化合价的变化;
Ⅱ、(1)依据反应前后电子守恒分析计算;
(2)①单线桥表示出该反应的电子转移,是标明电子转移方向和数目;
②依据化学方程式,结合氧化还原反应的概念进行计算;
点评:本题考查了化学反应类型的分析判断,氧化还原反应的概念判断,化学方程式的书写,氧化还原反应的电子转移计算和单线桥表示,电子守恒是氧化还原反应常用计算依据.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目