摘要:30.t℃时.纯水的KW=1×10-13.计算: (1)该温度下0.005mol/L的H2SO4溶液中:①C(H+) = mol/L ②C(OH-)= mol/L ③由水电离出的H+浓度= mol/L. (2)该温度下将0.005mol/L的H2SO4溶液和0.03mol/L的NaOH溶液按体积比为1:1混合.求混合后溶液的PH.
网址:http://m.1010jiajiao.com/timu3_id_290009[举报]
|
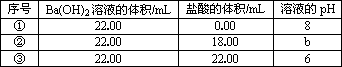
在t℃时,纯水中由水电离出的c(H+)和c(OH-)的乘积等于10-12.向该温度下某Ba(OH)2的稀溶液中逐滴加入同温下pH=a的盐酸,测得混合溶液的部分pH如下表如示:
假设混合前后溶液的体积变化忽略不计,则a、b的值分别为 | |
| [ ] | |
A. |
3、6.3 |
B. |
4、7 |
C. |
5、7 |
D. |
6、7.3 |
(6分)150℃时,只含C、H、O三种元素的有机物A 8.8 g 在一定量的O2中燃烧,生成的混合气体缓慢通过盛有足量无水CuSO4的干燥管,干燥管中的固体增重10.8g,剩余的气体通入盛有足量澄清石灰水的试剂瓶,试剂瓶中的物质增重8.8g,最后的气体缓慢通过盛有灼热CuO的硬质试管,硬质试管中的物质质量减少4.8g。请通过计算和分析回答下列问题:
⑴写有机物的分子式 ▲
⑵本题中,A和O2反应的化学方程式为 ▲ ;
⑶ 若A的结构满足下列条件:能和Na反应但不能和NaOH反应;能进行催化氧化但不能发生消去反应。则A的结构简式为 ▲ ;
查看习题详情和答案>>
(6分)室温时10mL某气态烃与过量的氧气混合,完全燃烧后的产物通过浓硫酸,再恢复到至室温,气体体积减少了50 mL ,剩余气体再通过氢氧化钠溶液,体积又减少了40 mL 。求气态烃的分子式并写出该分子式的所有同分异构体。
查看习题详情和答案>>