网址:http://m.1010jiajiao.com/timu3_id_288537[举报]
某学生拟通过测定粗锌(杂质与稀硫酸不反应)与稀硫酸反应产生的气体体积,来测定粗锌中锌的纯度。现用粗锌、稀硫酸、试管、镊子、单孔橡皮塞、导气管、托盘天平、量筒、水槽、铁架台(附铁夹)等仪器、药品进行实验。实验装置如图所示(固定装置未画出):

(1)该反应的离子方程式为 。
(2)某学生欲用11.9 mol/L 浓硫酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀硫酸。该学生需要用量筒量取 mL上述浓硫酸进行配制。
(3)实验时除需测定粗锌的质量、氢气的体积之外,是否还需要其他物理量?如需要,请指出____________________,否则,此空不填。
(4)在加入药品之前需检查装置气密性,如何检查该装置的气密性:
。
(5)以下是测量收集到气体体积必须包括的几个步骤:
①调整量筒内外液面高度使之相同;
②使试管和量筒内的气体都冷却至室温;
③读取量筒内气体的体积。
这三步操作的正确顺序是:________________________(请填写步骤代号)。
(6)如果实验中测得粗锌质量为a g,得到的氢气体积是b L(已折算成标准状况),水蒸气的影响忽略不计,粗锌中锌的质量分数的计算式为(用含a、b的代数式表示,不必化简):___________________。
(7)请提出另一种更简捷的实验方案:________________________________。
查看习题详情和答案>>某金属冶炼厂的管道烟泥中含有炭黑及金属铜、锌、硫.综合实践活动小组的同学设计了从管道烟泥中回收金属铜并利用废气中的二氧化硫制备硫酸的实验方案,实验过程如图所示: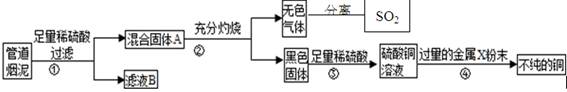
请回答:
(1)步骤①中,过滤操作使用了玻璃棒,其作用是 ;如何确定硫酸已经过量 。
(2)步骤④中,所加入的金属X与Zn的活动性顺序是Zn>X,金属X具有广泛用途,X是 ,有关反应的化学方程式 。
(3)除去不纯铜中的杂质金属X,可选用的试剂或用品有 (填标号)。
a.磁铁 b.稀盐酸 c.蒸馏水 d.氯化铜溶液.
(4)将分离出的SO2通过下列碘循环工艺过程既能制H2SO4,又能制取H2,其流程如下: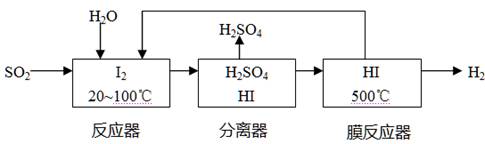
试写出反应器、膜反应器中的化学反应方程式 、 。
某金属冶炼厂的管道烟泥中含有炭黑及金属铜、锌、硫.综合实践活动小组的同学设计了从管道烟泥中回收金属铜并利用废气中的二氧化硫制备硫酸的实验方案,实验过程如图所示:
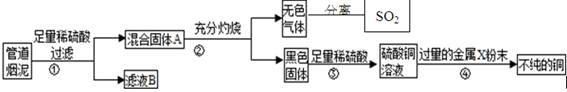
请回答:
(1)步骤①中,过滤操作使用了玻璃棒,其作用是 ;如何确定硫酸已经过量 。
(2)步骤④中,所加入的金属X与Zn的活动性顺序是Zn>X,金属X具有广泛用途,X是 ,有关反应的化学方程式 。
(3)除去不纯铜中的杂质金属X,可选用的试剂或用品有 (填标号)。
a.磁铁 b.稀盐酸 c.蒸馏水 d.氯化铜溶液.
(4)将分离出的SO2通过下列碘循环工艺过程既能制H2SO4,又能制取H2,其流程如下:
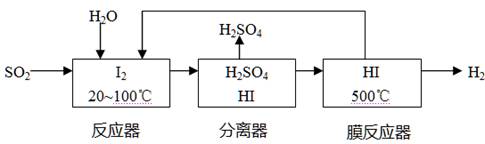
试写出反应器、膜反应器中的化学反应方程式 、 。
查看习题详情和答案>>
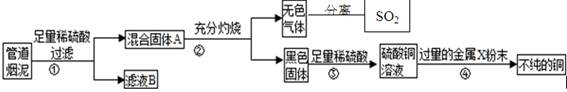
请回答:
(1)步骤①中,过滤操作使用了玻璃棒,其作用是 ;如何确定硫酸已经过量 。
(2)步骤④中,所加入的金属X与Zn的活动性顺序是Zn>X,金属X具有广泛用途,X是 ,有关反应的化学方程式 。
(3)除去不纯铜中的杂质金属X,可选用的试剂或用品有 (填标号)。
a.磁铁 b.稀盐酸 c.蒸馏水 d.氯化铜溶液.
(4)将分离出的SO2通过下列碘循环工艺过程既能制H2SO4,又能制取H2,其流程如下:

试写出反应器、膜反应器中的化学反应方程式 、 。
A.《物质结构与性质》:原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36.已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输.已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示.

①W元素基态原子价电子排布式为______.
②已知CN-与______分子互为等电子体,1molCN-中π键数目为______.
③上述沉淀溶解过程的化学方程式为______.
B.《化学实验》:无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂,工业上作防腐剂、制造白色颜料(锌钡白)等.某实验小组欲用制氢废液制备硫酸锌晶体,进行了以下实验:
(1)取50mL制氢废液,过滤.除去不溶性杂质后,用ZnO调节滤液使pH约等于2,加热、蒸发、浓缩制得较高温度下的硫酸锌饱和溶液,冷却结晶,得到粗制的硫酸锌晶体.
①加入少量氧化锌调节滤液使pH≈2目的是______;
②加热蒸发、浓缩溶液时,应加热到______时,停止加热.
(2)粗晶体在烧杯中用适量蒸馏水溶解,滴加1~2滴稀硫酸,用沸水浴加热至晶体全部溶解.停止加热,让其自然冷却、结晶.抽滤(装置如图2所示).将所得晶体用少量无水乙醇洗涤1-2次,得到较纯的硫酸锌晶体.
①写出下列仪器的名称.a______;b______.
②抽滤跟普通过滤相比,除了得到沉淀较干燥外,还有一个优点是______.
③用少量无水乙醇洗涤晶体的目的是______.
(3)在制取氢气时,如果锌粒中混有少量的铁、铜杂质,对硫酸锌的质量______(填“有”、“无”)影响,原因是______.
查看习题详情和答案>>