摘要:把15g大理石高温加热直至没有气体放出.并依次如表5-3实验.称其剩余固体的质量(杂 质不反应不挥发),有关结果记录如表5-3. 表5-3 通入紫色石蕊试液 通入澄清石灰水 称量剩余物 溶液变为红色 石灰水变浑浊,物质总质量增加4.4g 剩余固体重9.06g (1)什么物质使紫色石蕊变红?写出有关化学方程式. (2)求大理石中碳酸钙的质量分数. 答案:(1)碳酸使之变红 CO2+ H2O= H2CO3 (2)设大理石中碳酸钙的质量分数为x mCO2=15 g-9.06 g=5.94 g CaCO3CaO+CO2↑ 100 44 15 g·x 5.94 g x=90% 第5单元知识网络
网址:http://m.1010jiajiao.com/timu3_id_28666[举报]
 大理石是重要的建筑材料.为了测定某大理石样品中杂质的含量,某实验小组准确称取100g样品,设计了如下实验方案:
大理石是重要的建筑材料.为了测定某大理石样品中杂质的含量,某实验小组准确称取100g样品,设计了如下实验方案:【实验一】将100g大理石样品放入硬质玻璃管中高温加热,在不同反应时间测得的实验数据如下表(大理石高温加热的反应方程式是:CaCO3
| ||
| 反应时间/min | 0 | 5 | 9 | 12 | 15 |
| 剩余固体质量/g | 100 | 91.2 | 73.6 | 64.8 | 64.8 |
35.2
35.2
g.(2)100g大理石样品中杂质的质量是多少克?(写出计算过程)
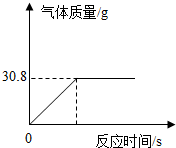
【实验二】将100g大理石样品放入一定量的稀盐酸中,充分反应后测得实验数据如图(杂质不与稀盐酸反应,气体的溶解忽略不计):
根据实验及有关数据进行分析:
(3)实验小组根据【实验二】数据计算出样品中杂质的质量为30g.经检查无计算原理及数字运算错误.请判断【实验二】的测定结果是否正确,如不正确要指出错误的原因.
该过程中的碳酸钙没有完全参加反应
该过程中的碳酸钙没有完全参加反应
. 大理石是重要的建筑材料.为了测定某大理石样品中杂质的含量,某实验小组准确称取100g样品,设计了如下实验方案:
大理石是重要的建筑材料.为了测定某大理石样品中杂质的含量,某实验小组准确称取100g样品,设计了如下实验方案:
【实验一】将100g大理石样品放入硬质玻璃管中高温加热,在不同反应时间测得的实验数据如下表(大理石高温加热的反应方程式是:CaCO3 CaO+CO2↑,杂质不反应):
CaO+CO2↑,杂质不反应):
| 反应时间/min | 0 | 5 | 9 | 12 | 15 |
| 剩余固体质量/g | 100 | 91.2 | 73.6 | 64.8 | 64.8 |
(2)100g大理石样品中杂质的质量是多少克?(写出计算过程)
【实验二】将100g大理石样品放入一定量的稀盐酸中,充分反应后测得实验数据如图(杂质不与稀盐酸反应,气体的溶解忽略不计):
根据实验及有关数据进行分析:
(3)实验小组根据【实验二】数据计算出样品中杂质的质量为30g.经检查无计算原理及数字运算错误.请判断【实验二】的测定结果是否正确,如不正确要指出错误的原因.______. 查看习题详情和答案>>
大理石是重要的建筑材料.为了测定某大理石样品中杂质的含量,某实验小组准确称取100g样品,设计了如下实验方案:
【实验一】将100g大理石样品放入硬质玻璃管中高温加热,在不同反应时间测得的实验数据如下表(大理石高温加热的反应方程式是:CaCO3 CaO+CO2↑,杂质不反应):
CaO+CO2↑,杂质不反应):
(1)100g大理石样品完全分解生成气体的质量是______g.
(2)100g大理石样品中杂质的质量是多少克?(写出计算过程)
【实验二】将100g大理石样品放入一定量的稀盐酸中,充分反应后测得实验数据如图(杂质不与稀盐酸反应,气体的溶解忽略不计):
根据实验及有关数据进行分析:
(3)实验小组根据【实验二】数据计算出样品中杂质的质量为30g.经检查无计算原理及数字运算错误.请判断【实验二】的测定结果是否正确,如不正确要指出错误的原因.______.
 查看习题详情和答案>>
查看习题详情和答案>>
【实验一】将100g大理石样品放入硬质玻璃管中高温加热,在不同反应时间测得的实验数据如下表(大理石高温加热的反应方程式是:CaCO3
 CaO+CO2↑,杂质不反应):
CaO+CO2↑,杂质不反应):| 反应时间/min | 5 | 9 | 12 | 15 | |
| 剩余固体质量/g | 100 | 91.2 | 73.6 | 64.8 | 64.8 |
(2)100g大理石样品中杂质的质量是多少克?(写出计算过程)
【实验二】将100g大理石样品放入一定量的稀盐酸中,充分反应后测得实验数据如图(杂质不与稀盐酸反应,气体的溶解忽略不计):
根据实验及有关数据进行分析:
(3)实验小组根据【实验二】数据计算出样品中杂质的质量为30g.经检查无计算原理及数字运算错误.请判断【实验二】的测定结果是否正确,如不正确要指出错误的原因.______.
 查看习题详情和答案>>
查看习题详情和答案>>
某同学将过量的木炭粉与少量的氧化铜粉混合,装入试管中,高温加热一段时间后,试管里有铜和未反应的木炭.为了得到纯净的铜,该同学把此混合物置于蒸发皿里强热,以便使木炭与氧气反应而除去.请回答:
(1)写出木炭与氧化铜反应的化学方程式 .
(2)你认为该同学能达到目的吗? (答“能”或“不能”),理由是 .
查看习题详情和答案>>
(1)写出木炭与氧化铜反应的化学方程式
(2)你认为该同学能达到目的吗?
某同学用木炭粉与氧化铜高温加热至质量不再变化为止,发现剩余固体中含一些黑色粉末,该同学取少量固体于试管中,加入足量稀硫酸,发现黑色固体全部溶解,溶液呈蓝色.
(1)剩余固体中的黑色粉末为 .
(2)为测定剩余固体中黑色粉末的质量分数,该同学称量5g剩余固体于烧杯中,再把25g稀硫酸平均分5次加入烧杯中,充分反应后烧杯中剩余固体的质量记录如下:
求:①黑色粉末在剩余固体中的质量分数.
②所加稀硫酸的溶质质量分数. 查看习题详情和答案>>
(1)剩余固体中的黑色粉末为
(2)为测定剩余固体中黑色粉末的质量分数,该同学称量5g剩余固体于烧杯中,再把25g稀硫酸平均分5次加入烧杯中,充分反应后烧杯中剩余固体的质量记录如下:
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀硫酸质量(g) | 5 | 5 | 5 | 5 | 5 |
| 烧杯中剩余固体质量(g) | 4.6 | 4.2 | 3.8 | 3.5 | 3.5 |
②所加稀硫酸的溶质质量分数. 查看习题详情和答案>>