摘要:18.把干燥.纯净的高锰酸钾和氯酸钾的混合物27 g装入大试管中加热制取氧气.当反应不再产生气体为止.待试管冷却后加入定量的水.溶解.过滤.滤出不溶物干燥后称重.质量为4.35g.求原混合物中氯酸钾的质量分数.生成氧气在标准状况下的体积是多少升?(标准状况下氧气密度为1.429 g/L) 提示:当反应不再产生气体时.意味着KMnO4和KClO3已完全分解.反应后的不溶物经处理后称质量为4.35 g.实际上是分解产生的MnO2的质量.由此可求出KMnO4及其产生氧气的质量.由高锰酸钾的质量可求KClO3的质量.由KClO3的质量可求其分解产生的氧气的质量.KMnO4和KClO3分解产生的氧气的质量之和为反应生成氧气的总质量.由氧气的质量及密度可求氧气的体积. 中考链接
网址:http://m.1010jiajiao.com/timu3_id_28664[举报]
把干燥、纯净的高锰酸钾和氯酸钾的混合物
27克装入大试管中加热制取氧气.当反应不再产生气体为止,待试管冷却后加入定量的水,溶解、过滤.滤出不溶物干燥后称重,质量为4.35克,求原混合物中氯酸钾的质量分数,生成氧气在标准状况下的体积是多少升?(标准情况下氧气密度为1.429g/L) 查看习题详情和答案>>请结合下图回答问题:

(1)写出图中有标号仪器的名称:①
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是(填字母编号,以下同)
(3)二氧化碳的密度比空气大,能溶于水.实验室常用石灰石和稀盐酸在常温下反应制取二氧化碳,应选用的发生装置是
(4)F是一种可用于集气、洗气等的多功能装置.若将F装置内装满水,再连接量筒,用可用于测定不溶于水且不与水反应的气体体积,测量时气体应从
查看习题详情和答案>>

(1)写出图中有标号仪器的名称:①
酒精灯
酒精灯
;(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是(填字母编号,以下同)
A
A
,原因是高锰酸钾是固体,反应条件是加热
高锰酸钾是固体,反应条件是加热
,写出该反应的文字表达式高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
;用加热氯酸钾的方法制取氧气,应选用的发生装置是| 加热 |
A
A
,写出该反应的化学方程式2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
;用分解过氧化氢的方法制取氧气,应选用的发生装置是
| ||
| △ |
B
B
,写出该反应的化学方程式2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.若要收集较为纯净的氧气最好选用
| ||
E
E
装置;若要收集较为干燥的氧气最好选用C
C
装置,检验收集满的方法把带火星的小木条放在集气瓶口,若木条复燃,则氧气已集满
把带火星的小木条放在集气瓶口,若木条复燃,则氧气已集满
(3)二氧化碳的密度比空气大,能溶于水.实验室常用石灰石和稀盐酸在常温下反应制取二氧化碳,应选用的发生装置是
B
B
,收集装置是C
C
.实验室用加热熟石灰和氯化铵的方法制取氨气,应先用的发生装置是A
A
.(4)F是一种可用于集气、洗气等的多功能装置.若将F装置内装满水,再连接量筒,用可用于测定不溶于水且不与水反应的气体体积,测量时气体应从
b
b
(填“a”或“b”)进入F中.
请根据下列装置如图1,回答问题:

(1)写出标号①②的仪器名称:① ,② .
(2)某同学想要用高锰酸钾制制取一瓶较干燥的氧气,他应该选择 组合.装置A还需做的一点改动是 ,写出高锰酸钾制取氧气的化学方程式 .
(3)如果选择BD组合可以制取 气体,写出该反应的化学方程式 .
(4)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过溶解、过滤、 干燥就能得到纯净的二氧化锰固体.
(5)把(4)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是 .
(6)若选择装置F作为制取氢气的发生装置,其优点是 .如果如图2所示的装置来收集一瓶氧气,验满时应该将带火星的木条放在 .(选填“a”或“b”)导管口处. 查看习题详情和答案>>

(1)写出标号①②的仪器名称:① ,② .
(2)某同学想要用高锰酸钾制制取一瓶较干燥的氧气,他应该选择 组合.装置A还需做的一点改动是 ,写出高锰酸钾制取氧气的化学方程式 .
(3)如果选择BD组合可以制取 气体,写出该反应的化学方程式 .
(4)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过溶解、过滤、 干燥就能得到纯净的二氧化锰固体.
(5)把(4)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是 .
(6)若选择装置F作为制取氢气的发生装置,其优点是 .如果如图2所示的装置来收集一瓶氧气,验满时应该将带火星的木条放在 .(选填“a”或“b”)导管口处. 查看习题详情和答案>>
请根据下列装置如图1,回答问题:
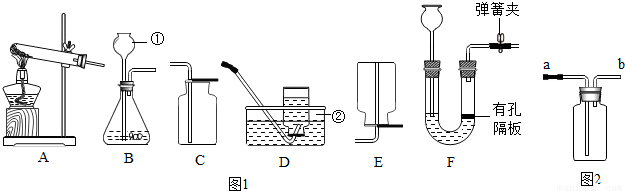
(1)写出标号①②的仪器名称:① ,② .
(2)某同学想要用高锰酸钾制制取一瓶较干燥的氧气,他应该选择 组合.装置A还需做的一点改动是 ,写出高锰酸钾制取氧气的化学方程式 .
(3)如果选择BD组合可以制取 气体,写出该反应的化学方程式 .
(4)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过溶解、过滤、 干燥就能得到纯净的二氧化锰固体.
(5)把(4)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是 .
(6)若选择装置F作为制取氢气的发生装置,其优点是 .如果如图2所示的装置来收集一瓶氧气,验满时应该将带火星的木条放在 .(选填“a”或“b”)导管口处. 查看习题详情和答案>>

(1)写出标号①②的仪器名称:① ,② .
(2)某同学想要用高锰酸钾制制取一瓶较干燥的氧气,他应该选择 组合.装置A还需做的一点改动是 ,写出高锰酸钾制取氧气的化学方程式 .
(3)如果选择BD组合可以制取 气体,写出该反应的化学方程式 .
(4)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过溶解、过滤、 干燥就能得到纯净的二氧化锰固体.
(5)把(4)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是 .
(6)若选择装置F作为制取氢气的发生装置,其优点是 .如果如图2所示的装置来收集一瓶氧气,验满时应该将带火星的木条放在 .(选填“a”或“b”)导管口处. 查看习题详情和答案>>
(2013?中山二模)请根据下列装置如图1,回答问题:

(1)写出标号①②的仪器名称:①
(2)某同学想要用高锰酸钾制制取一瓶较干燥的氧气,他应该选择
(3)如果选择BD组合可以制取
(4)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过溶解、过滤、
(5)把(4)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是
(6)若选择装置F作为制取氢气的发生装置,其优点是
查看习题详情和答案>>

(1)写出标号①②的仪器名称:①
长颈漏斗
长颈漏斗
,②水槽
水槽
.(2)某同学想要用高锰酸钾制制取一瓶较干燥的氧气,他应该选择
AC
AC
组合.装置A还需做的一点改动是在试管口放一团棉花
在试管口放一团棉花
,写出高锰酸钾制取氧气的化学方程式2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.
| ||
(3)如果选择BD组合可以制取
氧气或氢气
氧气或氢气
气体,写出该反应的化学方程式2H2O2
2H2O+O2↑(或Zn+H2SO4═ZnSO4+H2↑)
| ||
2H2O2
2H2O+O2↑(或Zn+H2SO4═ZnSO4+H2↑)
.
| ||
(4)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过溶解、过滤、
洗涤
洗涤
干燥就能得到纯净的二氧化锰固体.(5)把(4)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是
搅拌,防止液体受热不均而飞溅
搅拌,防止液体受热不均而飞溅
.(6)若选择装置F作为制取氢气的发生装置,其优点是
可以控制反应的发生和停止
可以控制反应的发生和停止
.如果如图2所示的装置来收集一瓶氧气,验满时应该将带火星的木条放在b
b
.(选填“a”或“b”)导管口处.