摘要:22. Ⅰ.铜与稀硝酸反应的离子方程式为 ,在做铜与稀硝酸反应的实验时.常观察到试管内生成的气体先为浅红棕色.其原因是 ,为了能直接观察到生成的气体的颜色.可在往稀硝酸中加入铜的同时.加入少量碳酸盐.那么加入少量碳酸盐的作用是 . Ⅱ.某研究性学习小组欲证明:在同温同压下.相同浓度.相同体积的酸性不同的一元酸与足量镁带反应时.生成氢气的体积相同而反应速率不同.同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如下图.该实验的主要操作步骤如下: ①配制浓度均为1 mol·L-1盐酸和醋酸溶液, ②量取15.00 mL 1 mol·L-1盐酸和醋酸溶液分别加入两个锥形瓶中, ③分别称取除去表面氧化膜的镁带a g.并系于铜丝末端, ④在广口瓶中装足量的水.按图连接好装置.检查装置的气密性, ⑤将铜丝向下移动.使足量镁带浸入酸中.至反应完全.记录相关数据, ⑥反应结束后待温度恢复到室温.调整乙和丙中液面使二者处于同一平面.读出量筒中水的体积为V mL. 请你参与实验并回答下列问题: (1)量取15.00 mL 1 mol·L-1盐酸和醋酸溶液所用的仪器是 , A.带刻度的烧杯 B.量筒 C.酸式滴定管 D.碱式滴定管 (2)步骤③中a的数值至少是 ,步骤④中检查该装置气密性的操作与观察方法是: ,步骤⑤中应记录的数据是 , (3)本实验装置丙中量筒的规格是 . A.10mL B.100 mL C.200 mL D.500 mL (4) 若水蒸气的影响忽略不计.在实验室条件下.气体摩尔体积的计算式为:Vm= ,(5)试简述速率不等的原因是 ,铜丝不与酸接触的原因是 . (6)试写出镁与醋酸溶液反应的离子方程式: .
网址:http://m.1010jiajiao.com/timu3_id_285767[举报]
 Ⅰ.铜与稀硝酸反应的离子方程式为
Ⅰ.铜与稀硝酸反应的离子方程式为在做铜与稀硝酸反应的实验时,常观察到试管内生成的气体先为浅红棕色,其原因是
为了能直接观察到生成的气体的颜色,可在往稀硝酸中加入铜的同时,加入少量碳酸盐,那么加入少量碳酸盐的作用是
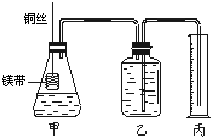
Ⅱ.某研究性学习小组欲证明:在同温同压下,相同浓度、相同体积的酸性不同的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如右图所示.该实验的主要操作步骤如下:
①配制浓度均为1mol?L-1盐酸和醋酸溶液;
②量取15.00mL 1mol?L-1盐酸和醋酸溶液分别加入两个锥形瓶中;
③分别称取除去表面氧化膜的镁带a g,并系于铜丝末端;
④在广口瓶中装足量的水,按图连接好装置,检查装置的气密性;
⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不与酸接触),至反应完全,记录相关数据;
⑥反应结束后待温度恢复到室温,调整乙和丙中液面使二者处于同一平面,读出量筒中水的体积为V mL.
请你参与实验并回答下列问题:
(1)量取15.00mL 1mol?L-1盐酸和醋酸溶液所用的仪器是
A.带刻度的烧杯 B.量筒 C.酸式滴定管 D.碱式滴定管
(2)步骤③中a的数值至少是
(3)本实验装置丙中量筒的规格是
A.10mL B.100mL C.200mL D.500mL
(4)若水蒸气的影响忽略不计,在实验室条件下,气体摩尔体积的计算式为:Vm=
(5)试简述速率不等的原因是
(6)试写出镁与醋酸溶液反应的离子方程式:
 某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:I. 取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3].
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状.
Ⅲ.按如图所示装置连接仪器、检查气密性、装入化学试剂.
(1)过程I发生反应的离子方程式是
Cu2(OH)2CO3+4H+═2Cu2++CO2↑+3H2O
Cu2(OH)2CO3+4H+═2Cu2++CO2↑+3H2O
.(2)写出过程Ⅲ中检查气密性的方法
打开b和a,关闭分液漏斗的活塞,将左边导管插入盛水的烧杯中,轻轻拉动注射器活塞,若导管中液面上升则说明气密性好
打开b和a,关闭分液漏斗的活塞,将左边导管插入盛水的烧杯中,轻轻拉动注射器活塞,若导管中液面上升则说明气密性好
.(3)过程Ⅲ的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是
产生红棕色气体
产生红棕色气体
,一段时间后使反应停止的操作是轻轻将注射器活塞向右拉使铜丝和溶液分开
轻轻将注射器活塞向右拉使铜丝和溶液分开
,关闭a,取下注射器.②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生.稀硝酸充满玻璃管的实验目是
将玻璃管中的NO2和空气排出
将玻璃管中的NO2和空气排出
,该反应的离子方程式是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如表所示(忽略温度对气体体积的影响):
| 实验编号 | 水温/℃ | 液面上升高度 | ||
| 1 | 25 | 超过试管的
| ||
| 2 | 50 | 不足试管的
| ||
| 3 | 0 | 液面上升超过实验1 |
低
低
(填“高”或“低”),进入试管中的溶液越多.②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO2 3HNO2=HNO3+2NO↑+H2O;
b.HNO2不稳定.
则产生上述现象的原因是
温度低,HNO2分解量减少,分解产生的NO气体量减少,所以进入试管的溶液多
温度低,HNO2分解量减少,分解产生的NO气体量减少,所以进入试管的溶液多
. 某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下:
某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下:
Ⅰ、取一段铜丝,用稀硫酸除去铜锈〔主要成分是 Cu2(OH)2CO3〕
Ⅱ、将洗涤后的铜丝做成匝数很多的螺旋状
Ⅲ、按如图所示连接仪器、检查气密性、装入化学试剂
(1)过程Ⅰ发生反应的离子方程式是______;
(2)过程Ⅱ将铜丝做成螺旋状的目的是______;
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触,操作是______.当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器.生成红棕色气体的化学方程式是______.
②控制b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体.稀硝酸充满玻璃管的实验目的是______.
(4)将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如下表所示:
| 实验编号 | 水温/0C | 液面上升高度 |
| 1 | 25 | 超过试管 |
| 2 | 50 | 不足试管 |
| 3 | 0 | 液面上升超过实验1 |
②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O═HNO2+HNO3 3HNO2═HNO3+2NO↑+H2O
b.HNO2不稳定.
产生上述现象的原因是______. 查看习题详情和答案>>
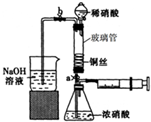 某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
I. 取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3].
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状.
Ⅲ.按如图所示装置连接仪器、检查气密性、装入化学试剂.
(1)过程I发生反应的离子方程式是______.
(2)写出过程Ⅲ中检查气密性的方法______.
(3)过程Ⅲ的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是______,一段时间后使反应停止的操作是______,关闭a,取下注射器.
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生.稀硝酸充满玻璃管的实验目是______,该反应的离子方程式是______.
(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如表所示(忽略温度对气体体积的影响):
| 实验编号 | 水温/℃ | 液面上升高度 |
| 1 | 25 | 超过试管的 |
| 2 | 50 | 不足试管的 |
| 3 | 0 | 液面上升超过实验1 |
②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO2 3HNO2=HNO3+2NO↑+H2O;
b.HNO2不稳定.
则产生上述现象的原因是______. 查看习题详情和答案>>
某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如下:
I. 取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
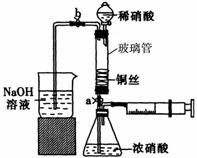 Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
III.按如图所示装置连接仪器、检查气密性、装入化学试剂。
(1)过程I发生反应的离子方程式是 。
(2)写出过程III中检查气密性的方法 。
⑶过程III的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是 ,一段时间后使反应停止的操作是 ,关闭a,取下注射器。
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生。稀硝酸充满玻璃管的实验目是 ,该反应的离子方程式是 。
(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):ks5u

①根据上表得出的结论是温度越 (填“高”或“低”),进入试管中的溶液越多。
②查阅资料:a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO2
3HNO2 =HNO3+2NO+H2O; b.HNO2不稳定。
则产生上述现象的原因是 。
查看习题详情和答案>>