摘要:29.工业生产硝酸的流程图如下 (1)已知N2(g) +3H2(g) 2NH3(g) , ΔH=-92.4kJ·mol-1.请回答: ① 当合成氨反应达到平衡后.改变某一外界条件(不改变N2.H2和NH3的量).反应速率与时间的关系如右图所示.图中tl 时引起平衡移动的条件可能是 . 其中表示平衡混合物中NH3的含量最高的一段时间是 . ②温度为T ℃时.将2a mol H2和a mol N2放入
网址:http://m.1010jiajiao.com/timu3_id_280648[举报]
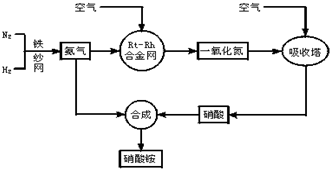
工业生产硝酸的流程图如下:

请回答下列问题:
(1)写出硝酸在工农业生产中的重要作用 (任写一条).
(2)已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ?mol-1.请回答:
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是 .
其中表示平衡混合物中NH3的含量最高的一段时间是 .
②温度为T℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该反应的化学平衡常数的为 .
(3)氨催化氧化的化学方程式为 ,该反应是放热反应,当温度升高时,反应的化学平衡常数K值 (增大、减小、无影响).
(4)今年“两会”后,党和国家更加重视环保.工业上常用纯碱溶液来吸收硝酸厂尾气中的二氧化氮,吸收产物中有亚硝酸钠、硝酸钠和二氧化碳,该化学方程式为 ;还可以利用氢气在催化剂下把氮的氧化物还原为 和水.
查看习题详情和答案>>

请回答下列问题:
(1)写出硝酸在工农业生产中的重要作用

(2)已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ?mol-1.请回答:
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是
其中表示平衡混合物中NH3的含量最高的一段时间是
②温度为T℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该反应的化学平衡常数的为
(3)氨催化氧化的化学方程式为
(4)今年“两会”后,党和国家更加重视环保.工业上常用纯碱溶液来吸收硝酸厂尾气中的二氧化氮,吸收产物中有亚硝酸钠、硝酸钠和二氧化碳,该化学方程式为
工业生产硝酸铵的流程图如下:

请回答下列问题:
(1)写出硝酸铵在工农业生产中的重要作用
(2)已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ?mol-1.请回答:
①在500℃、200atm和铁催化条件下向一密闭容器中充入1molN2和3molH2,充分反应后,放出的热量
.
②为有效提高氢气的转化率,宜采取的措施有
A.降低温度 B.最适合催化剂活性的适当高温 C.增大压强
D.降低压强 E.循环利用和不断补充氮气 F.及时移出氨
(3)一定温度下在体积固定的密闭容器中,将1mol N2和3mol H2混合,当该反应达到平衡时,测得平衡混合气的压强是反应前的0.85倍,此时N2的转化率为
查看习题详情和答案>>

请回答下列问题:
(1)写出硝酸铵在工农业生产中的重要作用
可做氮肥等
可做氮肥等
(任写一条)(2)已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ?mol-1.请回答:
①在500℃、200atm和铁催化条件下向一密闭容器中充入1molN2和3molH2,充分反应后,放出的热量
<
<
(填“<”“>”“=”)92.4kJ,该反应的化学平衡常数表达式K=| c2(NH3) |
| c3(H2)c(N2) |
| c2(NH3) |
| c3(H2)c(N2) |
②为有效提高氢气的转化率,宜采取的措施有
CEF
CEF
A.降低温度 B.最适合催化剂活性的适当高温 C.增大压强
D.降低压强 E.循环利用和不断补充氮气 F.及时移出氨
(3)一定温度下在体积固定的密闭容器中,将1mol N2和3mol H2混合,当该反应达到平衡时,测得平衡混合气的压强是反应前的0.85倍,此时N2的转化率为
30%
30%
.
如图是工业生产硝酸的流程.
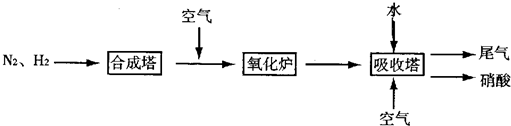
合成塔中内置铁触媒,氧化炉中内置Pt-Rh合金.请回答下列问题:
(1)1909年化学家哈伯在实验室首次合成了氨.2007年格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:

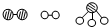 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别为 , .
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别为 , .
(2)已知N≡N的键能是946kJ?mol-1,H-H的键能为436kJ?mol-1,N-H的键能为393kJ?mol-1,写出合成塔中发生反应的热化学方程式 .
(3)已知4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=-1266.8kJ?mol-1;
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.8kJ?mol-1;
则热化学方程式N2(g)+O2(g)═2NO(g)△H= kJ?mol-1.
(4)吸收塔中通入空气的目的是 .
查看习题详情和答案>>

合成塔中内置铁触媒,氧化炉中内置Pt-Rh合金.请回答下列问题:
(1)1909年化学家哈伯在实验室首次合成了氨.2007年格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:

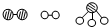 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别为
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别为(2)已知N≡N的键能是946kJ?mol-1,H-H的键能为436kJ?mol-1,N-H的键能为393kJ?mol-1,写出合成塔中发生反应的热化学方程式
(3)已知4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=-1266.8kJ?mol-1;
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.8kJ?mol-1;
则热化学方程式N2(g)+O2(g)═2NO(g)△H=
(4)吸收塔中通入空气的目的是
下图是工业生产硝酸的流程。

合成塔中内置铁触媒,氧化炉中内置Pt-Rh合金网。请回答下列问题:
⑴ 1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:

![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是 。
分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是 。
⑵ 合成氨反应的化学方程式为N2(g)+3H2(g)![]() 2NH3(g),写出该反应的化学平衡常数表达式K=
2NH3(g),写出该反应的化学平衡常数表达式K=
。在一定温度和压强下,将H2和N2按3∶1(体积比)混合后进入合成塔,反应达到平衡时,平衡混合气中NH3的体积分数为15%,此时H2的转化率为 。
⑶ 已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1266.8 kJ/mol
N2(g)+O2(g)=2NO(g) △H=+180.5 kJ/mol
氨催化氧化的热化学方程式为 。
⑷ 吸收塔中通入空气的目的是 。
查看习题详情和答案>>