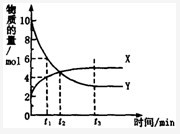
摘要: 在一定温度下.某容器内气体X.Y的物质的量随反应时间变化的曲线如右图所示.下列判断错误的是 A. t1时.c(Y)=2c(X) B. 反应的化学方程式为 2YX C. t2时.v(正)=v(逆).反应达到平衡状态 D. t3时.混合气体中X的体积分数为71.4 %
网址:http://m.1010jiajiao.com/timu3_id_278587[举报]
|
在一定温度下,向2 L某恒容密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g) | |
A. |
此时Y的浓度为0.6 mol/L |
B. |
5 min 内v(X)=0.06 mol/(L·min) |
C. |
容器内X、Y、Z的浓度之比为1∶2∶2时,则该反应达到平衡状态 |
D. |
只要反应时间足够长,X、Y就能完全转化为Z |
一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图。下列叙述中正确的是 

| A.反应的化学方程式为4X Y |
| B.当t1=2时,用X表示该反应在2min内的平均反应速率为0.25mol / (L·min) |
| C.t2时,正反应速率等于逆反应速率 |
| D.t3时,Y浓度不再变化,反应达到平衡 |
一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图。下列叙述中正确的是


A.反应的化学方程式为4X Y
B.当t1=2时,用X表示该反应在2min内的平均反应速率为0.25mol / (L·min)
C.t2时,正反应速率等于逆反应速率
D.t3时,Y浓度不再变化,反应达到平衡
查看习题详情和答案>>

 A. 反应的化学方程式为4X Y
A. 反应的化学方程式为4X Y