摘要:800℃时.向密闭容器中充入2mol CO2和5mol H2.发生反应: CO2(g)+H2(g)CO(g)+H2O(g) K=1.0 求CO2转化为CO的转化率. 长郡中学2008年下学期高二年级期终考试
网址:http://m.1010jiajiao.com/timu3_id_277305[举报]
 在一定体积的密闭容器中,进行如下化学反应:
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| [CO]?[H2O] |
| [CO2]?[H2] |
| [CO]?[H2O] |
| [CO2]?[H2] |
(2)该反应为
吸热
吸热
反应(选填“吸热”、“放热”).(3)若 830℃时,向容器中充入1mol CO、5mol H2O,反应达到平衡后,其化学平衡常数K
等于
等于
1.0(选填“大于”、“小于”、“等于”)(4)若1200℃时,在某时刻该容器中CO2、H2、CO、H2O的浓度分别为2mol?L-1、2mol?L-1、4mol?L-1、4mol?L-1,则此时上述反应的平衡移动方向为
逆反应方向
逆反应方向
.(选填“正反应方向”、“逆反应方向”、“不移动”)(5)科学家一直致力于“人工固氮”的方法研究.目前合成氨的技术原理为:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
该反应的能量变化如图所示.
①在反应体系中加入催化剂,反应速率增大,E2的变化是:
减小
减小
.(填“增大”、“减小”或“不变”).②将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生如下反应:N2(g)+3H2(g)?2NH3(g)
5分钟后达到平衡,测得N2为0.2mol,H2为0.6mol,NH3为0.2mol.氮气的平均反应速率v(N2)=
0.01mol/L?min
0.01mol/L?min
,H2的转化率是33.3%
33.3%
.③欲提高②容器中H2的转化率,下列措施一定可行的是
ACD
ACD
.A.增大压强
B.改变反应的催化剂
C.液化生成物分离出氨
D.向容器中按原比例再充入原料气
E.升高温度.
随着环保意识的增强,清洁能源越来越受人们关注.
(1)氢能在二十一世纪有可能在世界能源舞台上成为一种举足轻重的二次能源.
①硫-碘循环分解水制氢主要涉及下列反应:
I.SO2+2H2O+I2=H2SO4+2HIⅡ.2HI
H2+I2Ⅲ.2H2SO4=2SO2+O2+2H2O
分析上述反应,下列判断正确的是
a.反应Ⅲ易在常温下进行 b.反应I中SO2氧化性比HI强
c.循环过程中需补充H2O d.循环过程中产生l mol O2的同时产生1mol H2
②利用甲烷与水反应制备氢气,因原料价廉产氢率高,具有实用推广价值,已知该反应为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ?mol-1若800℃时,反应的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=3.0mol?L-1;c(H2O)=8.5mol?L-1;c(CO)=2.0mol?L-1;c(H2)=2.0mol?L-1,则此时正逆反应速率的关系是v正
③实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)
CH3OH(g)分析该反应并回答下列问题:
①下列各项中,不能说明该反应已达到平衡的是
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗1mol CO,同时生成l mol CH3OH
②如图甲是该反应在不同温度下CO的转化率随时间变化的曲线.T1和T2温度下的平衡常数大小关系是K1
③已知甲醇燃料电池的工作原理如图乙所示.
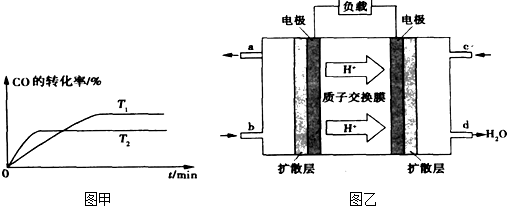
①该电池工作时,b口通入的物质为
查看习题详情和答案>>
(1)氢能在二十一世纪有可能在世界能源舞台上成为一种举足轻重的二次能源.
①硫-碘循环分解水制氢主要涉及下列反应:
I.SO2+2H2O+I2=H2SO4+2HIⅡ.2HI
| 通电 |
分析上述反应,下列判断正确的是
c
c
(填序号,下同).a.反应Ⅲ易在常温下进行 b.反应I中SO2氧化性比HI强
c.循环过程中需补充H2O d.循环过程中产生l mol O2的同时产生1mol H2
②利用甲烷与水反应制备氢气,因原料价廉产氢率高,具有实用推广价值,已知该反应为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ?mol-1若800℃时,反应的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=3.0mol?L-1;c(H2O)=8.5mol?L-1;c(CO)=2.0mol?L-1;c(H2)=2.0mol?L-1,则此时正逆反应速率的关系是v正
>
>
v逆.(填“>”、“<”或“=”)③实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡
向右
向右
移动(填“向左”、“向右”或“不”);若加入少量下列固体试剂中的b
b
,产生H2的速率将增大.a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)
| 加热 |
①下列各项中,不能说明该反应已达到平衡的是
d
d
.a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗1mol CO,同时生成l mol CH3OH
②如图甲是该反应在不同温度下CO的转化率随时间变化的曲线.T1和T2温度下的平衡常数大小关系是K1
>
>
K2.(填“>”、“<”或“=”)③已知甲醇燃料电池的工作原理如图乙所示.

①该电池工作时,b口通入的物质为
CH3OH
CH3OH
,该电池正极的电极反应式为:O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
,工作一段时间后,当6.4g甲醇(CH3OH)完全反应生成CO2时,有1.2
1.2
mol电子发生转移.合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H1=+206.1kJ/mol
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等.在相同温度下发生反应②,并维持反应过程中温度不变.已知甲容器中CH4的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象.
(3)反应CO(g)+H2O(g)?CO2(g)+H2(g) 800℃时,反应的化学平衡常数K=1.0.
①某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时反应中正、逆反应速率的关系式是
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
②800℃时,向体积为2L的密闭容器中充入2mol CO和4mol H2O,求达到平衡时CO的转化率.
查看习题详情和答案>>

请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为
5~10分钟、12分钟后
5~10分钟、12分钟后
;10min时,改变的外界条件可能是升高温度
升高温度
.(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等.在相同温度下发生反应②,并维持反应过程中温度不变.已知甲容器中CH4的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象.
(3)反应CO(g)+H2O(g)?CO2(g)+H2(g) 800℃时,反应的化学平衡常数K=1.0.
①某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
a
a
(填代号).a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
②800℃时,向体积为2L的密闭容器中充入2mol CO和4mol H2O,求达到平衡时CO的转化率.