网址:http://m.1010jiajiao.com/timu3_id_276404[举报]
 为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
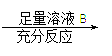 |
方案Ⅱ:铜铝混合物 测定剩余固体的质量
回答下列问题:
⑴小组成员一致认为两个方案都可行,你认为在实验室中选择方案 更便于实施。
⑵小组成员一致认为两个方案中可供选择的溶液A和B有很多,你认为在两个方案中溶液A和B均可选用的是 。(填编号)
A.稀盐酸 B.氢氧化钠溶液 C.硫酸铜溶液
⑶小组成员为探究Cu2+、Al3+在溶液中是否可以依次转化为沉淀而析出,设计了如下实验:向含有0.01molHNO3、0.001molCu(NO3)2、0.045molAl(NO3)3的溶液中逐滴加入一定浓度的NH3H2O溶液,使混合溶液的PH值不断升高,当加至溶液的体积为45 mL时Al3+开始反应生成成沉淀,当加至溶液的体积为50 mL时Cu2+开始反应生成沉淀。(不考虑溶液的体积变化)
【查阅资料】:常温下Ksp[Al(OH)3]=1.0×10-33mol·L-4,Ksp[Cu(OH)2]=2.0×10-20mol·L-3。
①Al(OH)3开始析出时溶液的PH值?
②若溶液中离子的浓度约为1.0×10-5 mol·L-时可视为沉淀完全,则当Al(OH)3沉淀完全时Cu(OH)2是否析出?
查看习题详情和答案>>为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
方案Ⅰ:铜铝混合物![]() 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物![]() 测定剩余固体的质量
测定剩余固体的质量
回答下列问题:
(1)小组成员一致认为两个方案都可行,你认为在实验室中选择方案 更便于实施。
(2)小组成员一致认为两个方案中可供选择的溶液A和B有很多,你认为在两个方案中溶液A和B均可选用的是 。(填编号)
A.稀盐酸 B.氢氧化钠溶液 C.硫酸铜溶液
(3)小组成员为探究Cu2+、Al3+在溶液中是否可以依次转化为沉淀而析出,设计了如下实验:向含有0.01molHNO3、0.001molCu(NO3)2、0.045molAl(NO3)3的溶液中逐滴加入一定浓度的NH3?H2O溶液,使混合溶液的PH值不断升高,当加至溶液的体积为45 mL时Al3+开始反应生成沉淀,当加至溶液的体积为50 mL时Cu2+开始反应生成沉淀。(不考虑溶液的体积变化)
[查阅资料]:常温下Ksp[Al(OH)3]=1.0×10-33mol?L-4,
Ksp[Cu(OH)2]=2.0×10-20mol?L-3。
请回答下列问题:
①Al(OH)3开始析出时溶液的PH应大于 。
②若溶液中离子的浓度约为1.0×10-5 mol?L-时可视为沉淀完全,则当Al(OH)3沉淀完全时Cu(OH)2是否析出?
查看习题详情和答案>>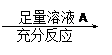 为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:方案Ⅰ:铜铝混合物 测定生成气体的体积
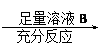 |
方案Ⅱ:铜铝混合物 测定剩余固体的质量
回答下列问题:
⑴小组成员一致认为两个方案都可行,你认为在实验室中选择方案 更便于实施。
⑵小组成员一致认为两个方案中可供选择的溶液A和B有很多,你认为在两个方案中溶液A和B均可选用的是 。(填编号)
A.稀盐酸 B.氢氧化钠溶液 C.硫酸铜溶液
⑶小组成员为探究Cu2+、Al3+在溶液中是否可以依次转化为沉淀而析出,设计了如下实验:向含有0.01molHNO3、0.001molCu(NO3)2、0.045molAl(NO3)3的溶液中逐滴加入一定浓度的NH3H2O溶液,使混合溶液的PH值不断升高,当加至溶液的体积为45mL时Al3+开始反应生成成沉淀,当加至溶液的体积为50mL时Cu2+开始反应生成沉淀。(不考虑溶液的体积变化)
【查阅资料】:常温下Ksp[Al(OH)3]=1.0×10-33mol·L-4,Ksp[Cu(OH)2]=2.0×10-20mol·L-3。
①Al(OH)3开始析出时溶液的PH值?
②若溶液中离子的浓度约为1.0×10-5 mol·L-时可视为沉淀完全,则当Al(OH)3沉淀完全时Cu(OH)2是否析出?
