网址:http://m.1010jiajiao.com/timu3_id_272852[举报]
(本小题15分)已知一定条件下丙烯的浓HBr能发生如下反应:
CH3-CH=CH2 + H-Br CH3--CH3
化合物A和A’互为同分异构体,元素分析含溴58.4%(其它元素数据不全,下同)。A和A’有如下系列反应,其中气态物质B是烃,含碳85.7%;C’不发生类似图中C的系列转化;E为酸性物质,其中碳氢含量共为63.6%。
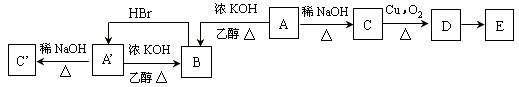
请回答下列问题:
(1)写出结构简式:A ,B: 。
(2)写出下列转化关系的化学方程式:
①B→A’ : 。
②C→D: 。
③D→E: 。
(3)简述检验A中含有溴元素的实验方法:
。
查看习题详情和答案>>(本小题15分)已知一定条件下丙烯的浓HBr能发生如下反应:
CH3-CH=CH2 + H-Br CH3--CH3
化合物A和A’互为同分异构体,元素分析含溴58.4%(其它元素数据不全,下同)。A和A’有如下系列反应,其中气态物质B是烃,含碳85.7%;C’不发生类似图中C的系列转化;E为酸性物质,其中碳氢含量共为63.6%。

请回答下列问题:
(1)写出结构简式:A ,B: 。
(2)写出下列转化关系的化学方程式:
①B→A’ : 。
②C→D: 。
③D→E: 。
(3)简述检验A中含有溴元素的实验方法: 。
查看习题详情和答案>>(本小题15分)为测定空气中CO2含量,做下述实验。
| 配0.1mol/L的标准盐酸和0.01mol/L的标准盐酸 | → | 用0.1mol/L的标准盐酸滴定未知Ba(OH)2溶液10mL用去盐酸19.60 mL | → | 用Ba(OH)2溶液吸收空气中的CO2 | → | 过 滤 | → | 取滤液20mL,用0.01mol/L的盐酸滴定用去盐酸34.8mL |
(1)为配置标准溶液,请选取必需的一组仪器 。
①托盘天平 ②容量瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒
A.①②⑤⑥ B.②④⑤⑥⑦ C.②①⑥⑦ D.②④⑤⑥
(2)滴定操作时,左手 ,眼睛注视 。
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤。需过滤的原因是 。
(4)由实验数据算出空气中CO2的体积分数为 。
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即更换溶液,进行第二次滴定,导致实验数据值(填偏高、偏低或无影响) 。
查看习题详情和答案>>(本小题15分) A、B、C、D四元素的核电荷数依次增加,它们的离子的电子层数相同且最外层电子数均为8。A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。回答以下问题:
(1)四元素的符号依次是A______;B______;C________;D______。
(2)写出B、D元素的离子结构示意图:
B.______________________; D.______________________。
(3)用电子式表示A、C元素形成的离子化合物的过程:
________________________________________________________。
(4)在A、B、C、D最高价氧化物水化物中:
比较其中酸的酸性强弱:____________________________;
比较其中碱的碱性强弱:____________________________。
查看习题详情和答案>>(本小题12分) A、B、C、D、E是五种短周期元素,原子序数依次增大。前四种的原子序数之和是E的原子序数的二倍。E的阳离子与D的阴离子都比A阳离子多2个电子层。D与四种元素中任意一种都可形成原子个数比不相同的若干种化合物。B是形成化合物种类最多的元素。请回答下列问题:
(1)写出元素符号:A________,E________。
(2)D在周期表中位于第_______周期第________族。
(3)五种元素原子半径由大到小的顺序是(用A~E字母表示)_______________。
(4)A、B、C、D可形成一种受热易分解的化合物,写出该化合物受热分解的化学方程式____________________________________________________________。
(5)A、B、D可形成A2B2D4型化合物,该化合物的名称是_____________。
查看习题详情和答案>>