摘要:下列有关实验操作或判断不正确的是 (填有关序号.选错倒扣分). A.用10 mL量筒量取稀硫酸溶液 8.0 mL B.分离苯和苯酚的混合液.先加入适量浓溴水.再过滤.分液.即可实现 C.用碱式滴定管量取KMnO4溶液 19.60 mL D.直接使用银氨溶液来检验淀粉的水解产物 E.为了测定某溶液的pH.将未经湿润的pH试纸浸入到待测溶液.过一会取出.与标准比色卡进行对比 F.用滴定管滴定标准液时.先俯视后仰视.会使滴定结果偏高 G.工业采用电解法精炼铜时.纯铜作阳极 将两铂片插入KOH溶液中作为电极.在两极区分别通入甲烷(或H2.CO等可燃性气体)和O2构成燃料电池.则通入甲烷气体的极是原电池的 极,通入O2的极为原电池的 极.该极的电极反应式为 .
网址:http://m.1010jiajiao.com/timu3_id_264765[举报]
(1)下列有关实验操作或判断不正确的是________(填有关序号,选错倒扣分).
A、用10mL量筒量取稀硫酸溶液8.0mL
B、用干燥的pH试纸测定氯水的pH
C、用碱式滴定管量取KMnO4溶液19.60mL
D、使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大
E、圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上
F、测定硫酸铜晶体中结晶水含量时,将加热后的坩埚置于干燥器中冷却后再称量
G.用冰醋酸,蒸馏水和容量瓶等仪器配制pH为1的醋酸稀溶液
(2)实验室利用如右图装置进行中和热的测定.

回答下列问题:
①该图中有两处未画出,它们是________、________;
②如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将(填“偏大”、“偏小”或“不变”);原因是________.
(3)在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:
2MnO4-+5C2O42-+16H+![]() 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
①用托盘天平称取WgNa2C2O4晶体.
②将WgNa2C2O4配成100mL标准溶液,移取20.00mL置于锥形瓶中,则酸性KMnO4溶液应装在________(填“酸式”或“碱式”)滴定管中.
③若滴定管的起始读数和终点读数如图所示,则酸性KMnO4的物质的量浓度为________(填表达式).
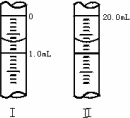
④若滴定完毕立即读数,测定的KMnO4溶液的浓度________(填“偏高”“偏低”或“不变”).
下列有关实验操作或判断不正确的是
A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大.
B.用干燥的pH试纸测定氯水的pH.
C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌.
D.100mL容量瓶可用于配制95mL 0.1mol/L NaCl溶液.
E.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量.
F.观察钾元素焰色反应的操作是:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察.
G.苯、CCl4、酒精可用来萃取溴水中的溴.
查看习题详情和答案>>
BEFG
BEFG
(填序号).A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大.
B.用干燥的pH试纸测定氯水的pH.
C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌.
D.100mL容量瓶可用于配制95mL 0.1mol/L NaCl溶液.
E.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量.
F.观察钾元素焰色反应的操作是:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察.
G.苯、CCl4、酒精可用来萃取溴水中的溴.
下列有关实验操作或判断不正确的是
A、配制一定物质的量浓度溶液,定容时俯视刻度线.
B、苯、四氯化碳、汽油三种有机溶剂都可用来萃取溴水中的溴.
C、让一束光通过胶体,从垂直于光线的方向可以看到一条光亮的“通路”.
D、用洁净干燥的玻璃棒蘸取溶液,滴在湿润的pH试纸上,跟标准比色卡比较测定溶液的pH.
E、配制100mL 1mol/L 的NaOH溶液,需称量4g 的氢氧化钠固体.
F、将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2.
查看习题详情和答案>>
A、D、E、F
A、D、E、F
(填序号,多选扣分).A、配制一定物质的量浓度溶液,定容时俯视刻度线.
B、苯、四氯化碳、汽油三种有机溶剂都可用来萃取溴水中的溴.
C、让一束光通过胶体,从垂直于光线的方向可以看到一条光亮的“通路”.
D、用洁净干燥的玻璃棒蘸取溶液,滴在湿润的pH试纸上,跟标准比色卡比较测定溶液的pH.
E、配制100mL 1mol/L 的NaOH溶液,需称量4g 的氢氧化钠固体.
F、将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2.