摘要:8.以下粒子只具有氧化性的是 A.Fe3+ B.Fe2+ C.Fe D. H2
网址:http://m.1010jiajiao.com/timu3_id_264635[举报]
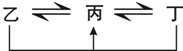 有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系:
有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系:①均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;
②均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应.
请回答下列问题:
(1)化合物甲的电子式为
(2)F元素在周期表中的位置
(3)均含有D元素的乙与丁在溶液中发生反应的离子方程式
(4)丙、丁分别是含F元素的简单阳离子,检验含丙、丁两种离子的混合溶液中的低价离子,可以用酸性KMnO4溶液,其对应的离子方程式为:
(5)已知常温下化合物FE的Ksp=6×10-18 mol2?L-2,常温下将1.0×10-5mol?L-1的Na2E溶液与含FSO4溶液按体积比3:2混合,若有沉淀FE生成,则所需的FSO4的浓度要求
(2000?上海)我国规定饮用水质量标准必须符合下列要求:
以下是源水处理成自来水的工艺流程示意图

(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式
(2)凝聚剂除去悬浮固体颗粒的过程
①只有物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4?7H2O常用的凝聚剂,它在水中最终生成
(3)通入二氧化碳的目的是
(4)气体A通常使用氯气,氯气的作用是基于其和水反应的产物之一具有
(5)下列物质中能作为氯气的代用品的是
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2.
查看习题详情和答案>>
| pH值 | 6.5-8.5 |
| Ca2+,Mg2+总浓度 | <0.0045mol/L |
| 细菌总数 | <100个/mL |

(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式
HCO3-+OH-=CO32-+H2O;
HCO3-+OH-=CO32-+H2O;
(2)凝聚剂除去悬浮固体颗粒的过程
③
③
(填写编号,多选倒扣)①只有物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4?7H2O常用的凝聚剂,它在水中最终生成
胶状Fe(OH)3
胶状Fe(OH)3
沉淀.(3)通入二氧化碳的目的是
除去Ca2+
除去Ca2+
和调节PH值
调节PH值
.(4)气体A通常使用氯气,氯气的作用是基于其和水反应的产物之一具有
强氧化
强氧化
性,请写出氯气与水反应的离子反应方程式Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
.(5)下列物质中能作为氯气的代用品的是
①③
①③
(填写编号,多选倒扣)①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2.
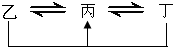 元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:
元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:(1)写出化合物甲的电子式:


(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式
3NH3?H2O+Al3+=Al(OH)3↓+3NH4+
3NH3?H2O+Al3+=Al(OH)3↓+3NH4+
;写出均含有F元素的乙与丁在溶液中发生反应的离子方程式Fe+2Fe3+=3Fe2+
Fe+2Fe3+=3Fe2+
.(3)由A、C元素组成的化合物戊和A、E元素组成的化合物己,式量均为34.其中戊的熔沸点高于己,其原因是:
H2O2分子间存在氢键
H2O2分子间存在氢键
.(4)复盐是指由2种或2种以上阳离子和一种酸根离子组成的盐.请写出由A、B、C、E、F元素组成的一种具有还原性的复盐庚的化学式
NH4)2Fe(SO4)2或(NH4)2Fe(SO4)2?6H2O或(NH4)2SO4?FeSO4?6H2O
NH4)2Fe(SO4)2或(NH4)2Fe(SO4)2?6H2O或(NH4)2SO4?FeSO4?6H2O
.该复盐是一种重要的化学试剂,据中学课本介绍,工业上常用如下方法制取:将一定量的两种盐配成混合溶液,再加热浓缩混合溶液,冷却至室温则析出带有6个结晶水的该复盐晶体.写出相关反应的化学方程式(NH4)2SO4+FeSO4+6H2O=(NH4)2Fe(SO4)2?6H2O
(NH4)2SO4+FeSO4+6H2O=(NH4)2Fe(SO4)2?6H2O
,析出该复盐晶体的原理是硫酸亚铁铵在水中溶解度比硫酸铵、硫酸亚铁在水中的溶解度要小得多
硫酸亚铁铵在水中溶解度比硫酸铵、硫酸亚铁在水中的溶解度要小得多
.