摘要:15].下列反应的离子方程式书写正确的是 A NaHCO3的水解:HCO3-+H2OH3O++CO32- B 硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O C 硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓ D 除去KNO3溶液中的Fe3+:Fe3++3H2OFe(OH)3↓+3H+
网址:http://m.1010jiajiao.com/timu3_id_264007[举报]
[化学-选修2:化学与技术]
草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产.一种制备草酸(含2个结晶水)的工艺流程如下:
回答下列问题:
(1)CO和NaOH在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程式分别为
(2)该制备工艺中有两次过滤操作,过滤操作①的滤液是
(3)工艺过程中③和④的目的是
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸.该方案的缺点是产品不纯,其中含有的杂质主要是
(5)结晶水合草酸成品的纯度用高锰酸钾法测定.称量草酸成品0.250g溶于水中,用0.0500mol?L-1的酸性KMnO4溶液滴定,至粉红色不消褪,消耗KMnO4溶液15.00mL,反应的离子方程式为
查看习题详情和答案>>
草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产.一种制备草酸(含2个结晶水)的工艺流程如下:

回答下列问题:
(1)CO和NaOH在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程式分别为
CO+NaOH
HCOONa
| ||
| 2MPa |
CO+NaOH
HCOONa
、
| ||
| 2MPa |
2HCOONa
Na2C2O4+H2↑
| △ |
2HCOONa
Na2C2O4+H2↑
.| △ |
(2)该制备工艺中有两次过滤操作,过滤操作①的滤液是
氢氧化钠溶液
氢氧化钠溶液
,滤渣是CaC2O4
CaC2O4
;过滤操作②的滤液是H2C2O4溶液
H2C2O4溶液
和H2SO4溶液
H2SO4溶液
,滤渣是CaSO4
CaSO4
.(3)工艺过程中③和④的目的是
分别循环利用氢氧化钠和硫酸来降低成本,减小污染
分别循环利用氢氧化钠和硫酸来降低成本,减小污染
.(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸.该方案的缺点是产品不纯,其中含有的杂质主要是
Na2SO4
Na2SO4
.(5)结晶水合草酸成品的纯度用高锰酸钾法测定.称量草酸成品0.250g溶于水中,用0.0500mol?L-1的酸性KMnO4溶液滴定,至粉红色不消褪,消耗KMnO4溶液15.00mL,反应的离子方程式为
5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O
5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O
;列式计算该成品的纯度94.5%
94.5%
.
学习化学应该明确“从生活中来,到生活中去”道理.在生产生活中,我们会遇到各种各样的化学反应.请按要求回答下列问题:
(1)写出下列反应的化学方程式.(注意反应条件并配平)
①镁带着火时,不能用液态CO2灭火剂来灭火的原因是 .
②工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉 .
(2)请你写出下列反应的离子方程式.
①胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多 .
②电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板 .
(3)工业上生产半导体材料硅的流程如图:
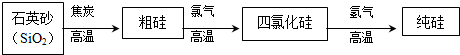
写出在制备粗硅时反应的化学方程式并标出电子转移的方向和数目: .
(4)铝热反应在工业生产中的重要用途之一是 ;小苏打在日常生活中的用途之一是 ,将小苏打和纯碱的混合物19.0g加热到恒重,测得固体质量为15.9g,则混合物中小苏打的质量分数为 .
查看习题详情和答案>>
(1)写出下列反应的化学方程式.(注意反应条件并配平)
①镁带着火时,不能用液态CO2灭火剂来灭火的原因是
②工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉
(2)请你写出下列反应的离子方程式.
①胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多
②电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板
(3)工业上生产半导体材料硅的流程如图:

写出在制备粗硅时反应的化学方程式并标出电子转移的方向和数目:
(4)铝热反应在工业生产中的重要用途之一是
 (1)写出实现下列变化的化学方程式,注明①②反应的类型.
(1)写出实现下列变化的化学方程式,注明①②反应的类型.①
CH2=CH2+Br2-CH2Br-CH2Br
CH2=CH2+Br2-CH2Br-CH2Br
,反应类型加成反应
加成反应
;②
nCH2=CH2 →

nCH2=CH2 →
,反应类型
加聚反应
加聚反应
;③
CH2=CH2+H2O
CH3CH2OH
| 一定条件 |
CH2=CH2+H2O
CH3CH2OH
;| 一定条件 |
④
CH2=CH2+3O2
2CO2+2H2O
| ||
CH2=CH2+3O2
2CO2+2H2O
.
| ||
(2)实验室制取乙烯的方程式为
CH3CH2OH
CH2=CH2+H2O
| 170℃ |
| 浓硫酸 |
CH3CH2OH
CH2=CH2+H2O
.混合原料时应将| 170℃ |
| 浓硫酸 |
浓硫酸
浓硫酸
倒入乙醇
乙醇
中,反应中浓硫酸的作用为催化剂
催化剂
和脱水剂
脱水剂
.加热时间过长混合液往往会变黑,这是因为浓硫酸使有机物碳化
浓硫酸使有机物碳化
,除去杂质气体应将制得的气体通过盛有氢氧化钠
氢氧化钠
溶液,该操作叫洗气
洗气
,反应的离子方为CO2+2NaOH=Na2CO3+H2O
CO2+2NaOH=Na2CO3+H2O
.