题目内容
学习化学应该明确“从生活中来,到生活中去”道理.在生产生活中,我们会遇到各种各样的化学反应.请按要求回答下列问题:(1)写出下列反应的化学方程式.(注意反应条件并配平)
①镁带着火时,不能用液态CO2灭火剂来灭火的原因是
②工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉
(2)请你写出下列反应的离子方程式.
①胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多
②电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板
(3)工业上生产半导体材料硅的流程如图:
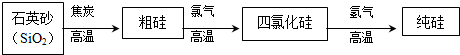
写出在制备粗硅时反应的化学方程式并标出电子转移的方向和数目:
(4)铝热反应在工业生产中的重要用途之一是
分析:(1)①镁能在二氧化碳中燃烧;
②氯气和消石灰反应生成氯化钙、次氯酸钙和水;
(2))①氢氧化铝能和酸反应生成盐和水;
②铁离子具有氧化性,能和铜发生氧化还原反应.
(3)高温下,碳还原二氧化硅制备粗硅;氧化还原反应中,化合价升高值=化合价降低值=转移电子数;
(4)铝热反应放出大量的热,可以用于焊接钢轨等;小苏打溶液呈溶解性,可以和酸反应,小苏打和纯碱的混合物加热发生反应2NaHCO3
Na2CO3+CO2↑+H2O,导致固体质量减少,根据方程式利用差量法计算NaHCO3的质量,进而计算Na2CO3的质量,据此解答.
②氯气和消石灰反应生成氯化钙、次氯酸钙和水;
(2))①氢氧化铝能和酸反应生成盐和水;
②铁离子具有氧化性,能和铜发生氧化还原反应.
(3)高温下,碳还原二氧化硅制备粗硅;氧化还原反应中,化合价升高值=化合价降低值=转移电子数;
(4)铝热反应放出大量的热,可以用于焊接钢轨等;小苏打溶液呈溶解性,可以和酸反应,小苏打和纯碱的混合物加热发生反应2NaHCO3
| ||
解答:解:(1)①镁在二氧化碳中燃烧生成氧化镁和碳2Mg+CO2
2MgO+C,碳又是可燃物,所以镁燃烧不能用液态二氧化碳灭火,故答案为:2Mg+CO2
2MgO+C;
②氯气和消石灰反应生成氯化钙、次氯酸钙和水,反应方程式为2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O,
故答案为:2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;
(2)①胃酸为盐酸,氢氧化铝能和盐酸发生中和反应而抑制胃酸过多,离子反应方程式为:Al(OH)3+3H+═Al 3++3H2O,
故答案为:Al(OH)3+3H+═Al 3++3H2O;
②铁离子具有氧化性,能和铜反应生成铜离子和亚铁离子,反应离子方程式为:2Fe3++Cu=Cu2++2Fe2+,
故答案为:2Fe3++Cu=Cu2++2Fe2+;
(3)高温下,碳还原二氧化硅制备粗硅,其反应方程式为:SiO2+2C
Si+2CO,化合价升高的元素是C,降低元素是Si,化合价升高值=化合价降低值=转移电子数=4,电子转移的情况为: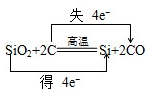 ,故答案为:
,故答案为: ;
;
(4)铝和其它金属氧化物发生铝热反应放出大量的热,该反应中铝为还原剂,所以铝热反应可以用于焊接钢轨或冶炼难熔金属等,小苏打是强碱弱酸酸式盐,能和胃酸反应生成氯化钠,且小苏打碱性较弱,可以治疗胃酸过多或作发酵粉,
设:混合物中含有xgNaHCO3,则:
2NaHCO3
Na2CO3+CO2↑+H2O 固体质量减少△m
2×84g 62g
xg 19.0gg-15.9g=3.1g
故
=
,解得x=8.4g,
所以:m(NaHCO3)=8.4g,
w(NaHCO3)=
×100%=44.2%,
故答案为:焊接钢轨或冶炼难熔金属等;发酵粉或治疗胃酸过多的药物;44.2%.
| ||
| ||
②氯气和消石灰反应生成氯化钙、次氯酸钙和水,反应方程式为2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O,
故答案为:2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;
(2)①胃酸为盐酸,氢氧化铝能和盐酸发生中和反应而抑制胃酸过多,离子反应方程式为:Al(OH)3+3H+═Al 3++3H2O,
故答案为:Al(OH)3+3H+═Al 3++3H2O;
②铁离子具有氧化性,能和铜反应生成铜离子和亚铁离子,反应离子方程式为:2Fe3++Cu=Cu2++2Fe2+,
故答案为:2Fe3++Cu=Cu2++2Fe2+;
(3)高温下,碳还原二氧化硅制备粗硅,其反应方程式为:SiO2+2C
| ||
 ,故答案为:
,故答案为: ;
;(4)铝和其它金属氧化物发生铝热反应放出大量的热,该反应中铝为还原剂,所以铝热反应可以用于焊接钢轨或冶炼难熔金属等,小苏打是强碱弱酸酸式盐,能和胃酸反应生成氯化钠,且小苏打碱性较弱,可以治疗胃酸过多或作发酵粉,
设:混合物中含有xgNaHCO3,则:
2NaHCO3
| ||
2×84g 62g
xg 19.0gg-15.9g=3.1g
故
| 2×84 |
| x |
| 62 |
| 3.1 |
所以:m(NaHCO3)=8.4g,
w(NaHCO3)=
| 8.4g |
| 19.0g |
故答案为:焊接钢轨或冶炼难熔金属等;发酵粉或治疗胃酸过多的药物;44.2%.
点评:本题考查了镁、铝、铁的性质,根据铁离子的氧化性、铝热反应等知识来分析解答,注意镁能在二氧化碳中燃烧,为易错点.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目