网址:http://m.1010jiajiao.com/timu3_id_263881[举报]
B.在次氯酸钙溶液中通入过量二氧化硫,其离子反应方程式为:Ca2++2ClO-+ 2H2O+2SO2 = Ca(HSO3)2+2HClO
C.常温下的溶液中Al3+、NH4+、Cl-、CO32-等离子可大量共存;
D.S(单斜)和S(正交)是硫的两种同素异形体,已知:
① S(单斜,s)+O2(g)== SO2(g);△H1=-297.16 kJ·mol-1
② S(正交,s)+O2(g)== SO2(g);△H2=-296.83 kJ·mol-1
则正交硫比单斜硫稳定;
(1)若发生大量氯气泄漏事故,下列措施中正确的是
a.立即通报相关部门,迅速撤离事故现场
b.用蘸有肥皂水的毛巾捂住口鼻立即逆风疏散
c.用蘸有NaOH溶液的毛巾捂住口鼻立即顺风疏散
(2)事故发生后,可用NaOH稀溶液处理泄漏的氯气,反应的离子方程式是
(3)实验室用氨气还原氧化铜的方法,通过测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)],测定铜的近似相对原子质量.反应的化学方程式是:2NH3+3CuO
| ||

①用上述装置制氨气时,能否将碳酸盐换成氯化铵?
②仪器从左到右的连接顺序(用字母编号表示,仪器可重复使用)是
C中的试剂是
③铜的相对原子质量是
| 18m(CuO) |
| m(H2O) |
| 18m(CuO) |
| m(H2O) |
(4)Cl2与NO2在一定条件下发生化合反应,生成一种气体,实验数据如图.图中横坐标是加入Cl2的物质的量,纵坐标是反应后气体物质的量总和.已知所取Cl2、NO2的物质的量总和为6mol.则生成物的化学式是

盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂.请回答下列问题:
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有________性.用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有________性.
(2)①在100 mL 18 mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是________.
A.40.32 L
B.30.24 L
C.20.16 L
D.13.44 L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式________.
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为________.
(4)分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出溶液呈“绿色”可能是溶液中Cu2+与NO2共存的结果,请你设计实验探究此说法正确与否(简述实验方案和实验现象及由此得出的结论)________.
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (K) |
7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 |
3.0×10-8 |
(2)25℃时,在20mL0.1mol?L-1氢氟酸中加入VmL0.1mol?L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示
 ,下列说法正确的是
,下列说法正确的是A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol?L-1
(3)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H=-akJ?mol-1,
②H+(aq)+OH-(aq)=H2O(l)△H=-bkJ?mol-1,
氢氟酸的电离方程式及热效应可表示为
(4)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与等物质的量的H2O反应得到HF和化合物A,则每生成1molHF转移
Ⅱ氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点-54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
SO2(g)+Cl2(g)
 SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1(1)试写出常温常压下化学平衡常数K的表达式:K=
(2)对上述反应,若要使化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是
a.降低温度 b.移走SO2Cl2
c.增加反应物浓度 d.无法满足上述条件
(3)下列描述中能说明上述反应已达平衡的是
a.υ(Cl2)=υ(SO2) b.容器中气体压强不随时间而变化
c.c(Cl2):c(SO2)=1:1 d.容器中气体颜色不随时间两变化
(4)300℃时,体积为1L的密闭容器中充入16.20g SO2Cl2,达到平衡时容器中含SO2 7.616g.若在上述中的平衡体系中,再加入16.20g SO2Cl2,当再次达平衡时,容器中含SO2的质量范围是
本题包括两个小题,共16 分。
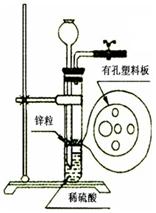
Ⅰ.某同学在实验室里利用一定量的Zn按右图所示的装置制取一定量的H2。在实验中他发现稀硫酸溶液不足而再无其他酸溶液可加入,经仔细思考后他通过长颈漏斗加入适量的某试剂完成了实验。下列试剂中他不可能选用的是(填写代码) 。
A.KCl溶液 B.酒精 C.苯 D.四氯化碳
Ⅱ.有甲、乙两学生分别按下面的步骤探究问题:在物质发生化学变化的前后,其总
质量是否发生增加或者减小或者不变?
(1)提出假设:物质发生化学变化的前后,其总质量不变。
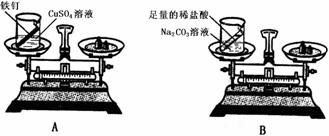
(2)设计方案并进行实验:甲设计的实验装置和选用药品如下图A所示,乙设计的实验装置和
选用药品如下图B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察。
①实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙认为:在化学反应中,生成物总质量与反应物总质量不相等。
②你认为 的结论正确。
③请从宏观的角度分析你认为正确的结论的原因 ;
④请从微观的角度分析你认为正确的结论的原因 ;
⑤请写出上述实验中有关反应的离子方程式
A ,B 。
查看习题详情和答案>>