网址:http://m.1010jiajiao.com/timu3_id_262586[举报]
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是
(1)试说明回收铝的过程中存在的困难。
(2)为什么金的回收率比铝的回收率要大得多?
(3)常温下,SiO2同强碱或强酸是很难反应的,现利用盐酸、氢氧化钠溶液、氮气、二氧化碳和水,从铝土矿中提取纯净的Al2O3。试设计一个适用于工业生产上提纯Al2O3的实验方案,用化学方程式表示提纯的过程。
(4)制取1 mol Al理论上需要多少库仑的电量?
(5)假定用6V的直流电源进行电解,制2.7吨铝需要多少千焦的电能?(请列式并计算)
(6)在1.01×105Pa,
(7)如果每度电的费用为0.60元,试计算生产厂家每生产1吨铝需付出的电费为多少元?(1度电=3 600 kJ)(请列式计算)
查看习题详情和答案>>铝可以从铝土矿中获取,铝土矿是不纯净的铝的氧化物(杂质为Fe2O3和SiO2),它是非再生资源.假如我们对铝的消费保持现有速度,我们能获得生产足够的铝所需的铝土矿仅能维持30年左右.由此看来,保护现有自然资源和对非再生资源的再利用,是值得我们考虑的.但是在废物回收过程中,仍有相当大的难度,其关键的因素主要涉及旧金属的收集与其他废物的分离、回收和提炼金属的费用、金属本身的价值等(已知1 mol电子电量荷约为105 C).
(1)试说明回收铝的过程中存在的困难.
(2)为什么金的回收率比铝的回收率要大得多?
(3)常温下,SiO2同强碱或强酸是很难反应的,现利用盐酸、氢氧化钠溶液、氮气、二氧化碳和水,从铝土矿中提取纯净的Al2O3.试设计一个适用于工业生产上提纯Al2O3的实验方案,用化学方程式表示提纯的过程.
(4)制取1 mol Al理论上需要多少库仑的电荷量?
(5)假定用6 V的直流电源进行电解,制2.7吨铝需要多少千焦的电能?(请列式并计算)
(6)在1.01×105 Pa,27℃时,每生产1 mol Al,理论上在阳极生成O2的体积为多少升?(请列式并计算)
(7)如果每度电的费用为0.60元,试计算生产厂家每生产1吨铝需付出的电费为多少元.(1度电=3600 kJ)(请列式计算)
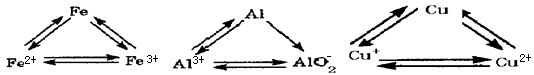
(1)氮化铝是一种性能良好的高温结构陶瓷,它的电子式:_________; 铁在周期表中的位置:_____________;
(2)铜生成铜绿是生活中常见的现象,其反应原理用方程式表示:_________; 氢氧化铝被称为两性氢氧化物,写出其酸式电离方程式:__________________;
(3)高铁酸盐被科学家们公认为绿色消毒剂, 它可以通过如下途径制备:次氯酸盐氧化法制备:采用次氯酸盐氧化法,在10.00 mL质量分数为8%的次氯酸钠溶液中加入5.5 g氢氧化钠和0.70 g硫酸铁,可制备摩尔浓度(物质的量浓度)为0.01 mol/L的高铁酸钠,写出制备的离子方程式: __________________高铁酸钠不仅可以消毒,也可以作净水剂,陈述理由:__________________
(4)燃料电池如图所示,写出石墨(I)电极上发生的电极反式:__________________ 。以此燃料电池作电源,以石墨为电极,电解一定浓度的CuSO4 溶液至无色后继续电解一段时间。断开电路,向溶液中加入0.1 mol Cu(OH)2,溶液恢复到电解之前的体积和浓度,则电解过程中转移电子的物质的量为_____________.。




铝可以从铝土矿中获取。铝土矿是不纯净的铝的氧化物(杂质为Fe2O3和SiO2),它是非再生资源。假如对铝的消费保持现有的速度,获得生产足够的铝所需的铝土矿仅能维持30年左右。由此看来,保护现有自然资源和对非再生资源的再利用,是值得考虑的。但废物回收有相当大的难度,其关键因素主要涉及旧金属的收集,与其他废物的分离、回收和提炼金属的费用,金属本身的价值等。(已知1 mol电子电量约为
(1)试说明回收铝的过程中存在的困难。
(2)为什么金的回收率比铝的回收率要大得多?
(3)常温下,SiO2与强碱或强酸是很难反应的。现利用盐酸、氢氧化钠溶液、氨气、二氧化碳和水,从铝土矿中提取纯净的Al2O3。试设计一个适用于工业Al2O3的实验方案。用化学方程式表示提纯的过程。
(4)制取1 mol Al需要多少库仑的电量?
(5)假定用6 V直流电源供电进行电解,制2.7 t Al需要多少千焦的电能?(请列式并计算)
查看习题详情和答案>>