网址:http://m.1010jiajiao.com/timu3_id_26198[举报]

(1)图1中,仪器b 的名称是______.
(2)实验室用高锰酸钾来装置制氧气时,应该选择的发生装置为______(填序号),选择该发生装置的依据是______,若用E装置收集氧气,当实验结束时实验结束时,甲同学先熄灭了酒精灯,忘记将导管从水中取出,在水未进入导管之前,可采取的补救措施有:①______ ②______.反应结束后冷却,对制取氧气后的固体残渣 (假定已完全反应,锰酸钾易溶于水) 作如下回收处理:
①通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是______(填写序号).
A.烘干 B.溶解 C.过滤 D.洗涤
②过滤、蒸发时都需用到的仪器是______(填序号).
A.酒精灯 B.烧杯 C.玻璃棒 D.漏斗
(3)小王同学欲收集一种难溶性气体,认为F装置可以代替E装置,那么小王在使用F装置时,操作过程中应先______,然后将产生的气体从______端 ( 填c或d ) 通入.
(4)图2 也可用于实验室制备二氧化碳的装置图.
在没有现成的二氧化碳气体发生器情况下,请你选用图3中部分仪器装配成一个能随开随用随关随停的二氧化碳气体发生装置,应选用合理的仪器是______.
(5)在查阅资料时,某小组的同学们得知氧化铁也可以作为过氧化氢分解制取氧气的催化剂,他们联想到MnO2可作为H2O2分解的催化剂,那么,氧化铁和二氧化锰这两种物质哪一种更适合呢?请你一起参与探究,完成下列问题.
【分析与探究】探究二氧化锰、氧化铁对过氧化氢分解速率的影响时,他们在控制变量的问题上提出了不同的观点,你认为不正确的是______.
A.过氧化氢溶液中溶质的质量分数一定相同 B.催化剂的质量一定相同
C.反应前过氧化氢溶液的温度一定相同 D.反应容器的容积一定相同
【实验验证】研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:用足量不同浓度的H2O2溶液制取相同体积O2所需的时间.
| 浓度 时间(min) 条件 | 30% | 15% | 5% |
| 加入ag | 0.2 | 0.8 | 2.0 |
| 加入ag | 7.0 | 9.0 | 16.0 |
查看习题详情和答案>>
实验室选用下列装置制取气体.根据要求回答问题:

(1)图l中仪器①的名称________,该装置中发生的化学方程式为________.图1装置也可以用于实验室制氧气,写出发生的化学方程式为________,该反应的类型是________.(填“化合反应”或“分解反应”)
(2)小杨同学将MnO2,与水泥按一定比例加水混合、凝固,制作成小块状固体,加入图2装置中制氧气,以方便实验结束后回收二氧化锰.实验前检查该装置气密性的方法是:打开旋塞,从长颈漏斗口注水至________,关闭旋塞,继续注水,使漏斗中液面略高于试管中液面,一段时间后,高度差不变,说明气密性良好.其中块状固体应放置在________处(填“A”或“B”).利用图2装置反应一段时间后,需停止反应,其操作是________.
(3)反应结束后冷却,对制取氧气后的固体残渣(假定已完全反应)作如下回收处理:
①通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是________(填写序号).
A.烘干
B.溶解
C.过滤
D.洗涤
②过滤、蒸发时都需用到的仪器是________(填序号).
A.酒精灯
B.烧杯
C.玻璃棒
D.漏斗
(4)若用装置图3制取气体过程中反应剧烈,从实验安全角度考虑,可采取的措施有________(填序号).
①用容积较小的锥形瓶
②控制液体的滴加速度
③加热反应物
④降低反应物浓度
(5)图4中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有________性质.这一性质在实际生活中的应用为________.
(6)在没有现成的二氧化碳气体发生器情况下,请你选用下图中部分仪器装配成一个能随开随用随关随停的二氧化碳气体发生装置,应选用合理的仪器是________.

NaCl、KNO3两种物质的溶解度曲线如下图所示。
①t1℃氯化钠的溶解度 (27) 硝酸钾(填“>”或“<”或“=”);
 ②图中a点的含义是 (28) ;
②图中a点的含义是 (28) ;
③若硝酸钾中含有少量氯化钠,要提 纯硝酸钾可
纯硝酸钾可
采用 (29) 的方法。
④某兴趣小组做了如下实验。
【实验一】提纯NaCl
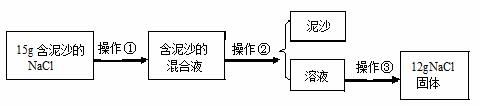
 请根据实验回答下列问题:
请根据实验回答下列问题:
Ⅰ.操作①、②、③依次为下图中的
(30) (填序号);
Ⅱ .若得到NaCl的产量比实际值偏低,则可能的原因是 (31) (填序号);
.若得到NaCl的产量比实际值偏低,则可能的原因是 (31) (填序号);
A.过滤时滤纸有破损,混合液流入滤液中
B.蒸发时受热不均匀,有晶体溅出
C.蒸发时,看到有晶体析出,立即停止加热
D.溶解15 g含有泥沙的NaCl样品时,加入的水量不足
Ⅲ.用上述实验所得纯净的氯化钠,配制5%的氯化钠溶液50 g,需要氯化钠 (32) g。
【实验 二】溶解和结晶
二】溶解和结晶
请根据硝酸钾的溶解度和相关实验,回答下列问题:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度(g/100g水) | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
某兴趣小组做了以下实验:
 Ⅳ. 上述溶液中的溶质是 (33) ,上述实验过程中得到的溶液一定属于
Ⅳ. 上述溶液中的溶质是 (33) ,上述实验过程中得到的溶液一定属于
不饱和溶液的是 (34) (填数字序号),⑤所对应的实验现象是 (35) ;
实验过程中,溶液中溶质的质量分数一定相等的是 (36) (填数字序号)。
Ⅴ.为了防止水体污染,小组同学提出了如下方案处理实验后的废液:
步骤I:将⑤继续冷却至0℃,过滤,共可回收得到KNO3固体 (37) g ;
步骤II:将步骤Ⅰ中的滤液(忽略过滤中的损耗)稀释,可得到 (38) g溶质质量分数为1%的KNO3溶液,用做肥料。
查看习题详情和答案>>(1)除去水样中难溶性的固体,需将水样(填序号)______;
①加热 ②过滤 ③蒸发 ④冷却
(2)有关水的组成和结构的叙述中,正确的是______ (填字母);
A.水中氢、氧元素的质量比为2:1
B.水是由水分子构成的
C.水分子是由氢分子和氧原子构成的
(3)欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是______.
(4)生活中为降低水的硬度并杀灭水中病原生物,可采用的方法是______.
(5)某同学在完成电解水实验时,发现正极产生了10mL气体,则负极产生的气体体积是______.该实验能够说明水是由氢元素与氧元素组成的理论依据是______.
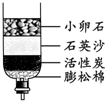
(6)用如图所示的简易净水器处理浑浊的河水,下面分析正确的是______
A.净水器能杀菌消毒
B.净化后的水属于纯净物
C.活性炭的主要作用是吸附
D.净水器能将硬水变为软水
(7)下列节水措施中不可取的是______
A.工业废水处理达标后循环使用
B.农业浇灌推广使用喷灌、滴灌技术
C.大量开采使用地下水
D.洗菜、淘米、洗衣的水可以用来浇花、拖地、冲厕所.

(1)操作①中必须用到的一种仪器是
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是

(3)操作⑤中除用到三脚架、酒精灯、玻璃棒、坩埚钳外,还需要用到
(4)如果过滤后得到的滤液仍然浑浊,请写出造成滤液浑浊的可能原因:
(5)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是
A.食盐没有全部溶解即过滤 B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿 D.器皿上沾有的精盐没全部转移到称量纸上.