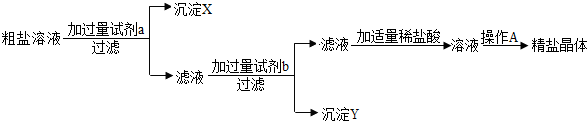
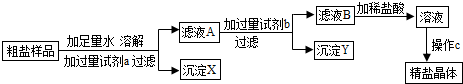
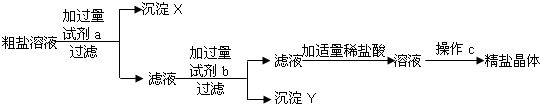
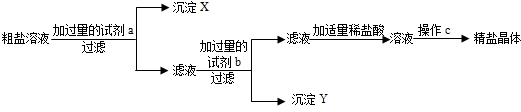
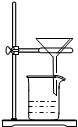
摘要: 某粗盐样品中含有杂质氯化镁.氯化钙.小林设计了以下提纯方案: (1)若方案中先除去的是氯化镁.接着除去氯化钙.回答: ①试剂a的化学式是 .b的化学式是 . ②指出操作c的名称 . ③操作过程中加适量稀盐酸时.可能发生的反应化学方程式是 . . (以上两个反应.顺序不分先后) (2)用图中所示装置进行过滤时.向过滤器内倾注液体的正确的方法是 A. 倾注时.玻璃棒插入过滤器中心 B. 倾注时.玻璃棒下端靠住过滤器内任意位置 C. 倾注时.玻璃棒下端靠住过滤器内三层滤纸一边 (3)若一次过滤后发现滤液仍浑浊.且滤纸未破损.需接着进行的操作是 . (4)若所取粗盐样品中实际含氯化钠的质量为mg.除杂后所得精盐的质量为ng.则m与n的关系是m n.原因是 .
网址:http://m.1010jiajiao.com/timu3_id_2596[举报]
某粗盐样品中含有杂质氯化镁、氯化钙、某同学设计了以下提纯方案:
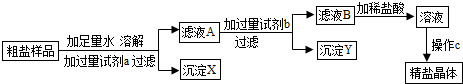
请回答下列问题:
(1)方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去粗盐中的
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到的仪器是
(3)醒制50g溶质质量分数为6%的NaCl溶液,需NaCI
(4)向滤液B滴加稀盐酸的过程中,当观察到的溶液的现象为
(5)操作C的名称为
A.蒸发时有一些液体、固体溅出
B.从蒸发皿将所得食盐晶体转移称量时有一定量残留往玻璃棒上
C.提纯后所得精盐尚未完全干燥.
(6)工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气、和氯气,写出反应的化学方程式
查看习题详情和答案>>

请回答下列问题:
(1)方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去粗盐中的
氯化镁
氯化镁
.(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到的仪器是
漏斗
漏斗
.(3)醒制50g溶质质量分数为6%的NaCl溶液,需NaCI
3
3
g,水47
47
ml.(4)向滤液B滴加稀盐酸的过程中,当观察到的溶液的现象为
刚刚无气泡产生
刚刚无气泡产生
时,应停止滴加,如果滴加的稀盐酸过量,对最后得到的精盐晶体的成分没有
没有
(填“有”或“没有”)影响.(5)操作C的名称为
蒸发
蒸发
;某同学所得精盐比其他同学明显要少,原因可能是AB
AB
.A.蒸发时有一些液体、固体溅出
B.从蒸发皿将所得食盐晶体转移称量时有一定量残留往玻璃棒上
C.提纯后所得精盐尚未完全干燥.
(6)工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气、和氯气,写出反应的化学方程式
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||