摘要: 下列在实验中可能遇到的意外事故处理正确的是 A. 苯着火时.用水来灭火 B. 金属钠着火燃烧时.用水灭火 C. 少量浓硫酸沾在皮肤上.立即用氢氧化钠溶液擦洗 D. 浓 NaOH 溶液溅到皮肤上.先用大量水冲洗.再涂上硼酸溶液
网址:http://m.1010jiajiao.com/timu3_id_258479[举报]
下图装置在有关气体的实验中经常用到(箭头表示进气)。

(1)③瓶在实验中可能起到的作用是_________________________________________。
(2)洗气需要用到的装置是__________________(填代号,下同)。用排水法测气体体积需要用到的装置是__________________。
查看习题详情和答案>>(1)氯水在和下列物质反应时,分别是氯水中哪种微粒在起主要作用?(写出其化学式)
①氯水与硝酸银溶液反应产生白色沉淀
②氯水中刚滴入石蕊试液时显红色
③氯水中加入碳酸钠产生无色气体
④氯化能使无水硫酸铜变蓝
⑤氯水中加镁粉,氯水的黄绿色会褪去
(2)氯水经光照后,pH值减小,该反应的化学方程式是
(3)在分别盛有NaCl溶液和NaI溶液的A、B两支试管中各加入1mL溴的CCl4溶液,用力振荡后再静止片刻.在A试管中出现的现象是
(4)工业上生产漂白粉的化学反应方程式为:
查看习题详情和答案>>
①氯水与硝酸银溶液反应产生白色沉淀
Cl-
Cl-
;②氯水中刚滴入石蕊试液时显红色
H+
H+
,过一段时间后,试液褪色HClO
HClO
;③氯水中加入碳酸钠产生无色气体
H+
H+
;④氯化能使无水硫酸铜变蓝
H2O
H2O
;⑤氯水中加镁粉,氯水的黄绿色会褪去
Cl2
Cl2
.(2)氯水经光照后,pH值减小,该反应的化学方程式是
2HClO
2HCl+O2↑
| ||
2HClO
2HCl+O2↑
.
| ||
(3)在分别盛有NaCl溶液和NaI溶液的A、B两支试管中各加入1mL溴的CCl4溶液,用力振荡后再静止片刻.在A试管中出现的现象是
下
下
层为CCl4层(填上或下),CCl4层呈棕红
棕红
色,B试管中的CCl4层呈紫
紫
色.试写出上述实验中可能发生的离子方程式Br2+2I -=2Br -+I2
Br2+2I -=2Br -+I2
.(4)工业上生产漂白粉的化学反应方程式为:
2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O
2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O
.漂白粉的有效成分是Ca(ClO)2
Ca(ClO)2
,用化学方程式表示漂白粉在空气中漂白的原理:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
.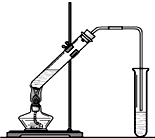 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:(1)乙醇、乙酸分子中的官能团分别是
(2)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止
(3)该反应属于哪类反应类型
A.加成反应 B.取代反应 C.水解反应
D.酯化反应 E.可逆反应
(4)写出制取乙酸乙酯的化学反应方程式
(5)无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸?
(6)乙醇在一定条件下还能发生脱水反应产生乙烯.乙烯通入溴的四氯化碳溶液中,观察到的现象是
此外,乙烯能用来生产环氧乙烷,生产工艺主要有两种:
工艺一:CH2=CH2+Cl2+O2→
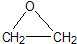 +CaCl2+H2O
+CaCl2+H2O工艺二:2CH2=CH2+O2
| Ag |
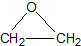
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,因此,在实际生产中,应采用
二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品.②有关物质的部分性质如下表:
设计实验装置图如下:
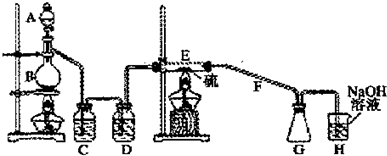
(1)图中气体发生和尾气处理装置不够完善,请你提出改进意见 .利用改进后的正确装置进行实验,请回答下列问题:
(2)仪器A、B的名称分别是 、 ;F的作用是 .
(3)C中的试剂是 ,其作用是 ;D中的试剂是 .其作用是 .
(4)E中反应的化学方程式: .
(5)如果在加热E时温度过高,对实验结果的影响是 ,在F中可能出现的现象是 .
(6)S2Cl2粗品中可能混有的杂质是(填写两种) 、 ,为了提高S2Cl2的纯度,关键的操作是控制好温度和 .
查看习题详情和答案>>
| 物质 | 熔点/℃ | 沸点/℃ | 化学性质 | ||||
| S | 112.8 | 444.6 | 略 | ||||
| S2Cl2 | -77 | 137 | 遇水生成HCl、SO2、S;300℃以上发生反应:S2Cl2+Cl2
|

(1)图中气体发生和尾气处理装置不够完善,请你提出改进意见
(2)仪器A、B的名称分别是
(3)C中的试剂是
(4)E中反应的化学方程式:
(5)如果在加热E时温度过高,对实验结果的影响是
(6)S2Cl2粗品中可能混有的杂质是(填写两种)
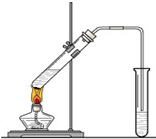 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:(1)乙醇、乙酸分子中的官能团分别是
羟基
羟基
、羧基
羧基
(2)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止
倒吸
倒吸
.(3)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是
防止暴沸
防止暴沸
.(4)该反应属于哪类反应类型
BDE
BDE
.A.加成反应 B.取代反应 C.水解反应 D.酯化反应 E.可逆反应
(5)写出制取乙酸乙酯的化学反应方程式
CH3COOH+CH3CH2OH
CH3COOC2H5+H2O
| 浓硫酸 |
| △ |
CH3COOH+CH3CH2OH
CH3COOC2H5+H2O
.| 浓硫酸 |
| △ |
(6)无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸?
水浴微热、用热毛巾热敷
水浴微热、用热毛巾热敷
.(7)乙醇在一定条件下还能发生脱水反应产生乙烯.乙烯通入溴的四氯化碳溶液中,观察到的现象是
溴水颜色褪去
溴水颜色褪去
;其反应方程式为CH2=CH2+Br-Br→CH2Br-CH2Br
CH2=CH2+Br-Br→CH2Br-CH2Br
.此外,乙烯能用来生产环氧乙烷,生产工艺主要有两种:
工艺一:
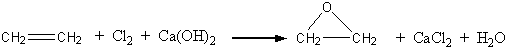
工艺二:
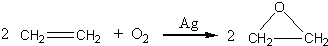
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,因此,在实际生产中,应采用
工艺二
工艺二
(填“工艺一”或“工艺二”)更环保、更经济.