摘要:NH3(g)燃烧生成NO2和H2O(g).已知 (1)2H2 ( g ) + O2 ( g ) = 2H2O ( g ) △H = -483.6 kJ/mol (2)N2 ( g ) + 2O2 ( g ) = 2NO2 ( g) △H = +67.8kJ/mol (3) N2 ( g ) + 3H2 ( g ) = 2NH3 ( g) △H = -92.0kJ/mol (4)H2O(l)=H2O(g), ΔH=+44kJ/mol 则NH3(g)的燃烧热是
网址:http://m.1010jiajiao.com/timu3_id_258132[举报]
 A、【供选学《化学与生活》考生作答】
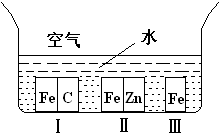
A、【供选学《化学与生活》考生作答】(1)如右图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是
(2)氟氯代烷是一种破坏臭氧层的物质.在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①Cl+O3→ClO+O2;②O3→O+O2;③ClO→Cl+O2
上列反应的总反应式是
(3)碳酸氢钠是常见的疏松剂,主要是因为它在加热条件下产生了气体,使食品变得疏松.试写出碳酸氢钠受热分解的化学方程式
(4)垃圾资源化的方法是
A、填埋 B、焚烧 C、堆肥法 D、分类回收法
B【供选学《化学反应原理》考生作答】
设反应①Fe(s)+CO2(g)═FeO(s)+CO(g)的平衡常数为K1.反应②Fe(s)+H2O(g)═FeO(s)+H2(g)的平衡常数K2,在不同温度下,K1、K2的值如下:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(2)现有反应③CO2(g)+H2(g)═CO(g)+H2O(g)写出该反应的平衡常数K3的数学表达式:K3═
(3)书写热化学方程式:
①1mol N2(g)与适量O2(g)起反应,生成NO2(g),吸收68KJ热量:
②NH3(g)燃烧生成NO2(g)和H2O(g),已知
(1)2H2(g)+O2(g)═2H2O(g)△H═-483.6kJ/mol
(2)N2(g)+2O2(g)═2NO2(g)△H═+67.8kJ/mol
1,N2(g)+3H2(g)═2NH3(g)△H═-92.0kJ/mol
NH3(g)燃烧生成NO2(g)和H2O (g)热化学方程式:
填空并写出下列反应的热化学方程式:
(1)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氧气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。
①写出肼和过氧化氢的电子式: 肼___________,过氧化氢___________ 。
②写出热化学方程式________________________。
③已知H2O(1)=H2O(g) △H=+44kJ/mol,则64g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是_________ kJ。
(2)NA表示阿伏加德罗常数,在CH4(g)完全燃烧生成CO2和液态水的反应中,每有
4NA个电子转移时,放出445kJ的热量。 _______________________________
(3)已知拆开1molN≡N键,1molH-H键,1molN-H键分别需要的能量是a kJ、b kJ、c kJ,则N2与H2反应生成NH3的热化学方程式为: ______________________________
(4)已知:
N2(g)+2O2(g)===2NO2(g) ΔH=+67.7 kJ/mol①
N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-543 kJ/mol②
1/2H2(g)+1/2F2(g)===HF(g) ΔH=-269 kJ/mol③
H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ/mol④
①写出肼(N2H4)和NO2反应的热化学方程式_____________________________________。
②有人认为若用氟气代替二氧化氮作氧化剂,则反应释放的能量更大,肼和氟气反应的热化学方程式为_________________________________。
查看习题详情和答案>>
(1)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氧气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。
①写出肼和过氧化氢的电子式: 肼___________,过氧化氢___________ 。
②写出热化学方程式________________________。
③已知H2O(1)=H2O(g) △H=+44kJ/mol,则64g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是_________ kJ。
(2)NA表示阿伏加德罗常数,在CH4(g)完全燃烧生成CO2和液态水的反应中,每有
4NA个电子转移时,放出445kJ的热量。 _______________________________
(3)已知拆开1molN≡N键,1molH-H键,1molN-H键分别需要的能量是a kJ、b kJ、c kJ,则N2与H2反应生成NH3的热化学方程式为: ______________________________
(4)已知:
N2(g)+2O2(g)===2NO2(g) ΔH=+67.7 kJ/mol①
N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-543 kJ/mol②
1/2H2(g)+1/2F2(g)===HF(g) ΔH=-269 kJ/mol③
H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ/mol④
①写出肼(N2H4)和NO2反应的热化学方程式_____________________________________。
②有人认为若用氟气代替二氧化氮作氧化剂,则反应释放的能量更大,肼和氟气反应的热化学方程式为_________________________________。
氨在国民经济中占有重要的地位.
(1)生成氢气:将水蒸气通过红热的炭即产生水煤气.
C(s)+H2O(g)?H2(g)+CO(g);△H=+131.3kJ/mol;△S=+133.7J/(mol?K).该反应在较低温度下能否自发进行______(填“能”或“不能”)
(2)已知在400°C时,2NH3(g)?N2(g)+3H2(g);△H>0的K=2.
①400°C时,N2(g)+3H2(g)?2NH3(g)的K=______(填数值)
②400°C时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时v(NH3)正______v(NH3)逆(填“大于”、“小于”、“等于”、“不确定”)
(3)体积相同的甲、乙两个容器中,分别充入等物质的量的氮气和氢气,在相同温度下发生反应N2(g)+3H2(g)?2NH3(g)并达到平衡,在这一过程中,甲容器保持体积不变,乙容器保持压强不变,则甲容器中氮气的转化率______乙容器中氮气的转化率(填“大于”、“小于”或“等于”)
(4)已知:1/2N2(g)+3/2H2(g)=NH3(g);△H=-46.0kJ/mol
H2(g)+1/2O2(g)=H2O(l);△H=-285.8kJ/mol
1/2N2(g)+O2(g)=NO2(g);△H=+33.9kJ/mol
H2O(l)=H2Og);△H=+44kJ/mol则氨气燃烧热的热化学方程式为______.
查看习题详情和答案>>
(1)生成氢气:将水蒸气通过红热的炭即产生水煤气.
C(s)+H2O(g)?H2(g)+CO(g);△H=+131.3kJ/mol;△S=+133.7J/(mol?K).该反应在较低温度下能否自发进行______(填“能”或“不能”)
(2)已知在400°C时,2NH3(g)?N2(g)+3H2(g);△H>0的K=2.
①400°C时,N2(g)+3H2(g)?2NH3(g)的K=______(填数值)
②400°C时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时v(NH3)正______v(NH3)逆(填“大于”、“小于”、“等于”、“不确定”)
(3)体积相同的甲、乙两个容器中,分别充入等物质的量的氮气和氢气,在相同温度下发生反应N2(g)+3H2(g)?2NH3(g)并达到平衡,在这一过程中,甲容器保持体积不变,乙容器保持压强不变,则甲容器中氮气的转化率______乙容器中氮气的转化率(填“大于”、“小于”或“等于”)
(4)已知:1/2N2(g)+3/2H2(g)=NH3(g);△H=-46.0kJ/mol
H2(g)+1/2O2(g)=H2O(l);△H=-285.8kJ/mol
1/2N2(g)+O2(g)=NO2(g);△H=+33.9kJ/mol
H2O(l)=H2Og);△H=+44kJ/mol则氨气燃烧热的热化学方程式为______.