摘要:29 (1)C2H5OH→C2H4↑+ H2O(条件浓硫酸.170oC肩头上写不上).消去反应 (2)C6H5–CH3+3HNO3→三硝基甲苯+3H2O 取代反应 (3)NH4++H2ONH3*H2O+OH-30. (1)A CH2=CH2 B C2H5OH C CH3COOH (2)B C .D Na 2CO2+2Na2O2=2Na2CO3+O2 31, (1) 吸热 (2) 减小
网址:http://m.1010jiajiao.com/timu3_id_257478[举报]
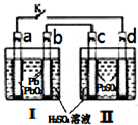 飞机、汽车、拖拉机、坦克,都是用蓄电池作为照明光源是典型的可充型电池,总反应式为:
飞机、汽车、拖拉机、坦克,都是用蓄电池作为照明光源是典型的可充型电池,总反应式为:Pb+PbO2+4H++2SO42-
| ||
| 充电 |
(1)当K闭合时,a电极的电极反应式是
PbO2+2e-+4H++SO42-=PbSO4+2H2O
PbO2+2e-+4H++SO42-=PbSO4+2H2O
;放电过程中SO42-向b
b
极迁移.当K闭合一段时间后,再打开K,Ⅱ可单独作为原电池使用,此时c电极的电极反应式为Pb-2e-+SO42-=PbSO4
Pb-2e-+SO42-=PbSO4
.(2)铅的许多化合物,色彩缤纷,常用作颜料,如铬酸铅是黄色颜料,碘化铅是金色颜料(与硫化锡齐名),室温下碘化铅在水中存在如下平衡:PbI2(S)?Pb2+(aq)+2I-(aq).
①该反应的溶度积常数表达式为Ksp=
c(Pb2+)?c2(I-)
c(Pb2+)?c2(I-)
.②已知在室温时,PbI2的溶度积Ksp=8.0×10-9,则100mL 2×10-3mol/L的碘化钠溶液中,加入100mL2×10-2mol/L的硝酸铅溶液,通过计算说明是否能产生PbI2沉淀
Qc=10-2?(10-3)2=10-8>Ksp,能产生PbI2沉淀
Qc=10-2?(10-3)2=10-8>Ksp,能产生PbI2沉淀
.③探究浓度对碘化铅沉淀溶解平衡的影响
该化学小组根据所提供试剂设计两个实验,来说明浓度对沉淀溶解平衡的影响.
提供试剂:NaI饱和溶液、NaCl饱和溶液、FeCl3饱和溶液、PbI2饱和溶液、PbI2悬浊液;
信息提示:Pb2+和Cl-能形成较稳定的PbCl42-络离子.
请填写下表的空白处:
| 实验内容 | 实验方法 | 实验现象及原因分析 |
| ①碘离子浓度增大对平衡的影响 | 取PbI2饱和溶液少量于一支试管中,再加入少量NaI饱和溶液, 取PbI2饱和溶液少量于一支试管中,再加入少量NaI饱和溶液, |
溶液中出现黄色浑浊. 原因是溶液中c(I-)增大,使Qc大于了pbI2的Ksp 溶液中出现黄色浑浊. 原因是溶液中c(I-)增大,使Qc大于了pbI2的Ksp |
| ②铅离子浓度减小对平衡的影响 | 取PbI2悬浊液少量于一支试管中,再加入少量NaCl饱和溶液 取PbI2悬浊液少量于一支试管中,再加入少量NaCl饱和溶液 |
黄色浑浊消失 原因是形成PbCl42-,导致溶液中c(Pb2+)减小,使Qc小于了pbI2的Ksp 黄色浑浊消失 原因是形成PbCl42-,导致溶液中c(Pb2+)减小,使Qc小于了pbI2的Ksp |
| ③ 铅离子和碘离子浓度都减小对平衡的影响 铅离子和碘离子浓度都减小对平衡的影响 |
在PbI2悬浊液中加入少量FeCl3饱和溶液 | PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 |
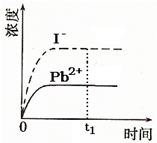 ④已知室温下PbI2的Ksp=8.0×10-9,将适量PbI2固体溶于 100mL水中至刚好饱和,该过程中Pb2+和I-浓度随时间变化关系如图(饱和PbI2溶液中c(I-)=0.0025mol?L-1).若t1时刻在上述体系中加入100mL.、0.020mol?L-1 NaI 溶液,画出t1时刻后Pb2+和I-浓度随时间变化关系图.
④已知室温下PbI2的Ksp=8.0×10-9,将适量PbI2固体溶于 100mL水中至刚好饱和,该过程中Pb2+和I-浓度随时间变化关系如图(饱和PbI2溶液中c(I-)=0.0025mol?L-1).若t1时刻在上述体系中加入100mL.、0.020mol?L-1 NaI 溶液,画出t1时刻后Pb2+和I-浓度随时间变化关系图.⑤至于碳酸铅,早在古代就被用作白色颜料.考古工作者发掘到的古代壁画或泥俑,其中人脸常是黑色的.经过化学分析和考证,证明这黑色的颜料是铅的化合物--硫化铅(已知PbCO3的
Ksp=1.46×10-13,PbS的Ksp=9.04×10-29)试分析其中奥妙
PbCO3的Ksp=1.46×10-13 >PbS的Ksp=9.04×10-29 故PbCO3与S2-接触时,转化为更难溶的黑色的PbS了
PbCO3的Ksp=1.46×10-13 >PbS的Ksp=9.04×10-29 故PbCO3与S2-接触时,转化为更难溶的黑色的PbS了
.Ⅰ.以硫铁矿为原料制取硫酸的生产中排出的废水对环境危害极大.酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表.
表1.几种砷酸盐的Ksp
表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]=
Ⅱ.“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ?m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
已知:①C(s)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1
②2H2(g)+O2(g)=2H2O(g)△H2=-483.6kJ?mol-1
③C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ?mol-1
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H=
标准状况下的煤炭气(CO、H2)33.6L与氧气完全反应生成CO2和H2O,反应过程中转移
查看习题详情和答案>>
表1.几种砷酸盐的Ksp
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As元素 |
| 浓度 | 28.42g/L | 1.6g?L-1 |
| 排放标准 | pH 6~9 | 0.5mg?L-1 |
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=
0.29
0.29
mol?L-1.(2)写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]=
c3(Ca2+)?c2 (AsO43-)
c3(Ca2+)?c2 (AsO43-)
,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol?L-1,c(AsO43-)的最大是5.7×10-17
5.7×10-17
mol?L-1.Ⅱ.“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ?m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
已知:①C(s)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1
②2H2(g)+O2(g)=2H2O(g)△H2=-483.6kJ?mol-1
③C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ?mol-1
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H=
-524.8
-524.8
kJ?mol-1.标准状况下的煤炭气(CO、H2)33.6L与氧气完全反应生成CO2和H2O,反应过程中转移
3
3
mol e-.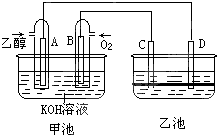 如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:
如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:(1)通入乙醇(C2H5OH)的惰性电极的电极反应式为
C2H5OH+16OH--12e-=2CO32-+11H2O
C2H5OH+16OH--12e-=2CO32-+11H2O
.若甲池可以充电,充电时A接电源的负极,此时B极发生的电极反应式为4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
.(2)在乙池反应过程中,可以观察到
C
C
电极周围的溶液呈现棕褐色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色,C极发生的电极反应式2I--2e?=I2
2I--2e?=I2
.(3)若在常温常压下,1gC2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1366.7kJ/mol
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1366.7kJ/mol
.(2013?兰州一模)乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制取:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H<0,请回答:
(1)在恒温、恒容的密闭容器中,下列描述能说明上述反应已达化学平衡状态的是
a.生成1mol CH3CH2OH的同时,生成3mol H2O
b.体系中各组份的物质的量浓度不随时间而变化
c.体系中混合气体的密度不随时间而变化
d.体系中气体的分子总数不随时间而变化
e.体系中的气体的总压强不随时间而变化
(2)上述反应的化学平衡常数的表达式为
.当温度T1>T2时,化学平衡常数K1
(3)在恒温、体积固定的某密闭容器中加入2mol CO2和6mol H2,达到平衡后测得CH3CH2OH为0.5mol,则H2的转化率为
(4)在工业生产中,可使H2的转化率和化学反应速率同时提高的措施有
(5)已知:0.5mol 乙醇液体燃烧生成二氧化碳和水蒸气,放出的热量为617.1kJ/mol,又知H2O(l)═H2O(g)△H=+44.2kJ/mol,请写出乙醇液体完全燃烧生成液态水的热化学方程式
查看习题详情和答案>>
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H<0,请回答:
(1)在恒温、恒容的密闭容器中,下列描述能说明上述反应已达化学平衡状态的是
bde
bde
(填字母序号).a.生成1mol CH3CH2OH的同时,生成3mol H2O
b.体系中各组份的物质的量浓度不随时间而变化
c.体系中混合气体的密度不随时间而变化
d.体系中气体的分子总数不随时间而变化
e.体系中的气体的总压强不随时间而变化
(2)上述反应的化学平衡常数的表达式为
| c3(H2O)?c(CH3OH) |
| c2(CO2)?c6(H2) |
| c3(H2O)?c(CH3OH) |
| c2(CO2)?c6(H2) |
<
<
K2(填“>”、“<”或“=”).(3)在恒温、体积固定的某密闭容器中加入2mol CO2和6mol H2,达到平衡后测得CH3CH2OH为0.5mol,则H2的转化率为
50%
50%
,如果再向该容器充入1mol CO2和3mol H2,平衡会向正向移动
正向移动
(填“正向移动”、“逆向移动”或“不移动”),再次达到平衡时,CO2的转化率会增大
增大
(填“增大”、“减小”或“不变”).(4)在工业生产中,可使H2的转化率和化学反应速率同时提高的措施有
增大CO2浓度或增大压强
增大CO2浓度或增大压强
(写出一条合理措施即可).(5)已知:0.5mol 乙醇液体燃烧生成二氧化碳和水蒸气,放出的热量为617.1kJ/mol,又知H2O(l)═H2O(g)△H=+44.2kJ/mol,请写出乙醇液体完全燃烧生成液态水的热化学方程式
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1366.8kJ/mol
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1366.8kJ/mol
.(2009?肇庆二模)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇:
①2CO2(g)+6H2(g)
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
②2CO(g)+4H2(g)
CH3CH2OH(g)+H2O(g) 25℃时,K=1.71×1022
(1)写出反应①的平衡常数表达式K=
.
(2)条件相同时,反应①与反应②相比,转化程度更大的是
(3)在一定压强下,测得反应①的实验数据如下表.分析表中数据回答下列问题:
①温度升高,K值
②提高氢碳比[n(H2)/n(CO2)],K值
(4)在右图的坐标系中作图说明压强变化对反应①的化学平衡的影响.并对图中横坐标、纵坐标的含义作必要的标注.
(5)肼(N2H4)与NO2反应生成N2和水蒸汽,比相同质量乙醇与O2燃烧生成CO2和水蒸汽产生的热能更多,故肼常作为高能火箭燃料.
已知:N2 (g)+2O2(g)═2NO2(g)△H=+67.7kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ/mol
则肼与二氧化氮反应生成氮气和水蒸汽的热化学方程式为:
查看习题详情和答案>>
①2CO2(g)+6H2(g)
| 催化剂 |
②2CO(g)+4H2(g)
| 催化剂 |
(1)写出反应①的平衡常数表达式K=
| c(C2H5OH)?c3(H2O) |
| c2(CO2)?c6(H 2) |
| c(C2H5OH)?c3(H2O) |
| c2(CO2)?c6(H 2) |
(2)条件相同时,反应①与反应②相比,转化程度更大的是
②
②
;以CO2为原料合成乙醇的优点是废弃物利用,有利于环保
废弃物利用,有利于环保
(写出一条即可).(3)在一定压强下,测得反应①的实验数据如下表.分析表中数据回答下列问题:
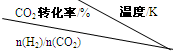 |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
减小
减小
(填“增大”、“减小”、或“不变”).
②提高氢碳比[n(H2)/n(CO2)],K值
不变
不变
(填“增大”、“减小”、或“不变”),对生成乙醇有利
有利
(填“有利”或“不利”).(4)在右图的坐标系中作图说明压强变化对反应①的化学平衡的影响.并对图中横坐标、纵坐标的含义作必要的标注.
(5)肼(N2H4)与NO2反应生成N2和水蒸汽,比相同质量乙醇与O2燃烧生成CO2和水蒸汽产生的热能更多,故肼常作为高能火箭燃料.
已知:N2 (g)+2O2(g)═2NO2(g)△H=+67.7kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ/mol
则肼与二氧化氮反应生成氮气和水蒸汽的热化学方程式为:
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7kJ
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7kJ
.