网址:http://m.1010jiajiao.com/timu3_id_256039[举报]
[2012·云南省质检](10分)用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去)。称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解。实验前量气管起始读数为amL,实验后量气管的最终读数为bmL。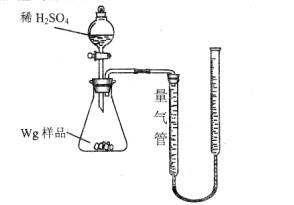
请回答下列问题:
(1)按上图完成装置连接,开始实验前必须进行的操作是 。
(2)写出锥形瓶中发生化合反应的离子方程式: 。
(3)实验结束后,锥形瓶内溶液中存在的金属离子有哪些可能?请根据选项进行填空(表格不一定填完):
| A.盐酸 | B.KSCN溶液 | C.酸性KMnO4溶液 | D.H2O2溶液 |
| 序号 | 溶液中可能存在 的金属离子 | 选择最少种数的试剂,验证该 假设(填字母) |
| ① | | |
| ② | | |
| ③ | | |
(5)若样品与足量稀硫酸反应后滴入KSCN溶液不显红色且量气管读数b>a(该实验条件下的气体摩尔体积为Vm)。下列有关单质铁质量分数的计算过程是否正确? (填“是”或“否”),理由是 。
Fe+H2SO4=FeSO4+H2↑
56g VmL
Wg×
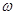 (Fe) (b-a)×10-3L
(Fe) (b-a)×10-3L……
 查看习题详情和答案>>
查看习题详情和答案>>
[2012·云南省质检](10分)用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去)。称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解。实验前量气管起始读数为amL,实验后量气管的最终读数为bmL。
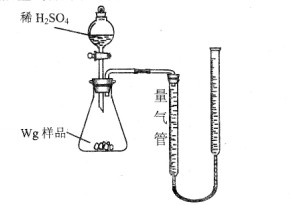
请回答下列问题:
(1)按上图完成装置连接,开始实验前必须进行的操作是 。
(2)写出锥形瓶中发生化合反应的离子方程式: 。
(3)实验结束后,锥形瓶内溶液中存在的金属离子有哪些可能?请根据选项进行填空(表格不一定填完):
A.盐酸 B.KSCN溶液 C.酸性KMnO4溶液 D.H2O2溶液
|
序号 |
溶液中可能存在 的金属离子 |
选择最少种数的试剂,验证该 假设(填字母) |
|
① |
|
|
|
② |
|
|
|
③ |
|
|
(4)实验中要对量气管多次读数,读数时应注意:①将实验装置恢复到室温;② ; ③视线与凹液面最低处相平。若读取量气管中气体的体积时,液面左高右低,则所测气体的体积 (填“偏大”、“偏小”或“无影响’”)。
(5)若样品与足量稀硫酸反应后滴入KSCN溶液不显红色且量气管读数b>a(该实验条件下的气体摩尔体积为Vm)。下列有关单质铁质量分数的计算过程是否正确? (填“是”或“否”), 理由是 。
Fe+H2SO4=FeSO4+H2↑
56g VmL
Wg×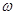 (Fe)
(b-a)×10-3L
(Fe)
(b-a)×10-3L
……
查看习题详情和答案>>

请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加
Na2SiO3溶液与过量的CO2反应的离子方程式为
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,体积) | 1.12 | 2.24 | 3.36 | 4.48 |
②滤渣B中Fe的质量分数为