题目内容
某同学拟定了以下实验方案,来确定一批合金废料的成分并加以回收利用.

请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加
Na2SiO3溶液与过量的CO2反应的离子方程式为
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
①实验①最先溶解的金属发生反应的化学方程式是
②滤渣B中Fe的质量分数为

请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和
Cu
Cu
(填化学式).(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为
H2O2(或O2)
H2O2(或O2)
;滤渣D、稀硫酸和试剂a总反应的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O
Cu+H2O2+H2SO4=CuSO4+2H2O
.(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加
过量盐酸,先有白色沉淀生成,继续滴加盐酸,白色沉淀全部溶解证明不不含硅酸钠
过量盐酸,先有白色沉淀生成,继续滴加盐酸,白色沉淀全部溶解证明不不含硅酸钠
.Na2SiO3溶液与过量的CO2反应的离子方程式为
SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-
SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-
.(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,体积) | 1.12 | 2.24 | 3.36 | 4.48 |
3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O
3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O
.②滤渣B中Fe的质量分数为
63.6%
63.6%
%(精确到0.1%).分析:(1)依据题干信息,结合(4)的溶解情况计算得到,最后得到蓝矾说明滤渣B中含有金属铜,证明合金中含有铜;
(2)双氧水是一种绿色氧化剂,可以实现金属铜和硫酸之间的反应;
(3)合金中的铝在过量氢氧化钠溶液中溶解生成偏铝酸钠和氢气,利用氢氧化铝溶于强酸溶液,硅酸不溶于酸设计实验验证;硅酸的酸性小于碳酸,二氧化碳过量反应生成碳酸氢钠;
(4))①金属铁的活泼性强于铜,根据金属铁和硝酸发生反应的情况来书写;
②先判断酸是否完全反应,再根据金属活动性判断反应的金属及生成的金属离子价态,根据1、2两组数据,结合采用极限法分析,确定剩余固体的成分,据此来计算即可.
(2)双氧水是一种绿色氧化剂,可以实现金属铜和硫酸之间的反应;
(3)合金中的铝在过量氢氧化钠溶液中溶解生成偏铝酸钠和氢气,利用氢氧化铝溶于强酸溶液,硅酸不溶于酸设计实验验证;硅酸的酸性小于碳酸,二氧化碳过量反应生成碳酸氢钠;
(4))①金属铁的活泼性强于铜,根据金属铁和硝酸发生反应的情况来书写;
②先判断酸是否完全反应,再根据金属活动性判断反应的金属及生成的金属离子价态,根据1、2两组数据,结合采用极限法分析,确定剩余固体的成分,据此来计算即可.
解答:解:(1)结合产物判断流程中生成蓝矾,说明B中含有铜,①由①、②两组数据分析,两次剩余物的质量相差4.2g,此时生成1.12LNO气体(转移0.075 mol电子).若只溶解铁,质量为4.2g,若只溶解铜,质量为4.8g.由此可知这9g中含有金属Cu,故答案为:Cu;
(2)双氧水是一种绿色氧化剂,在双氧水的作用下,金属铜可以和硫酸发生反应:Cu+H2O2+H2SO4+3H2O=CuSO4?5H2O或Cu+H2O2+H2SO4=CuSO4+2H2O,故答案为:Cu+H2O2+H2SO4+3H2O=CuSO4?5H2O或Cu+H2O2+H2SO4=CuSO4+2H2O;
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是利用氢氧化铝溶液强酸,硅酸不溶于强酸生成沉淀设计验证,方法为:取少量滤液A于试管中,滴加盐酸,开始生成白色沉淀为氢氧化铝,继续滴加盐酸,氢氧化铝会溶解生成氯化铝,无白色沉淀现象证明不含硅酸钠;过量二氧化碳通入硅酸钠溶液中,碳酸酸性大于硅酸,反应生成硅酸沉淀和碳酸氢钠,反应的离子方程式为:SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-;
故答案为:过量盐酸,先有白色沉淀生成,继续滴加盐酸,白色沉淀全部溶解证明不不含硅酸钠;SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-;
(4)①由①、②两组数据分析,两次剩余物的质量相差4.2g,此时生成1.12LNO气体(转移0.075 mol电子).若只溶解铁,质量为4.2g,若只溶解铜,质量为4.8g.由此可知这9g中是金属Cu,铁的还原性大于铜,所以铁先反应,实验①中发生反应的化学方程式为:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O,故答案为:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O;
②实验①有铜存在Fe3+会被还原为Fe2+,在金属消耗完毕以后,硝酸将亚铁离子氧化为三价铁,在亚铁离子转化为铁离子过程中,结合试验①可知还会产生4.48L-3.36L=1.12L的气体NO,物质的量为0.05mol,发生反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;可知反应的Fe2+物质的量为0.15mol,根据铁元素守恒,铁的质量分数=
×100%=63.6%;
故答案为:63.6%;
(2)双氧水是一种绿色氧化剂,在双氧水的作用下,金属铜可以和硫酸发生反应:Cu+H2O2+H2SO4+3H2O=CuSO4?5H2O或Cu+H2O2+H2SO4=CuSO4+2H2O,故答案为:Cu+H2O2+H2SO4+3H2O=CuSO4?5H2O或Cu+H2O2+H2SO4=CuSO4+2H2O;
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是利用氢氧化铝溶液强酸,硅酸不溶于强酸生成沉淀设计验证,方法为:取少量滤液A于试管中,滴加盐酸,开始生成白色沉淀为氢氧化铝,继续滴加盐酸,氢氧化铝会溶解生成氯化铝,无白色沉淀现象证明不含硅酸钠;过量二氧化碳通入硅酸钠溶液中,碳酸酸性大于硅酸,反应生成硅酸沉淀和碳酸氢钠,反应的离子方程式为:SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-;
故答案为:过量盐酸,先有白色沉淀生成,继续滴加盐酸,白色沉淀全部溶解证明不不含硅酸钠;SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-;
(4)①由①、②两组数据分析,两次剩余物的质量相差4.2g,此时生成1.12LNO气体(转移0.075 mol电子).若只溶解铁,质量为4.2g,若只溶解铜,质量为4.8g.由此可知这9g中是金属Cu,铁的还原性大于铜,所以铁先反应,实验①中发生反应的化学方程式为:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O,故答案为:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O;
②实验①有铜存在Fe3+会被还原为Fe2+,在金属消耗完毕以后,硝酸将亚铁离子氧化为三价铁,在亚铁离子转化为铁离子过程中,结合试验①可知还会产生4.48L-3.36L=1.12L的气体NO,物质的量为0.05mol,发生反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;可知反应的Fe2+物质的量为0.15mol,根据铁元素守恒,铁的质量分数=
| 0.15mol×56g/mol |
| 13.2g |
故答案为:63.6%;
点评:本题考查了物质定量测定的实验方法应用,物质性质的应用和判断是解题关键,数据分析和计算是难点,主要考查了铁、铝、铜及其化合物性质的综合应用和分离方法,题目难度较大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
某同学拟定了以下实验方案,来确定一批合金废料的成分并加以回收利用。

请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和____(填化学式)。
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为____;滤渣D、稀硫酸和试剂a总反应的化学方程式为 。
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加 。
Na2SiO3溶液与过量的CO2反应的离子方程式为 。
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
|
实验编号 |
① |
② |
③ |
④ |
|
稀HNO3体积(mL) |
100 |
200 |
300 |
400 |
|
剩余金属质量(g) |
9.0 |
4.8 |
0 |
0 |
|
NO体积(L,标况) |
1.12 |
2.24 |
3.36 |
4.48 |
①实验①最先溶解的金属发生反应的化学方程式是 。
②滤渣B中Fe的质量分数为____%(精确到0.1%)。
某同学拟定了以下实验方案,来确定一批合金废料的成分并加以回收利用.
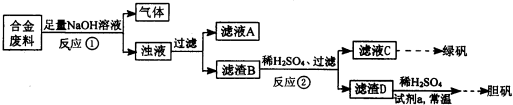
请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和______(填化学式).
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为______;滤渣D、稀硫酸和试剂a总反应的化学方程式为______.
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加______.
Na2SiO3溶液与过量的CO2反应的离子方程式为______.
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,体积) | 1.12 | 2.24 | 3.36 | 4.48 |
②滤渣B中Fe的质量分数为______%(精确到0.1%).
某同学拟定了以下实验方案,来确定一批合金废料的成分并加以回收利用.

请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和______(填化学式).
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为______;滤渣D、稀硫酸和试剂a总反应的化学方程式为______.
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加______.
Na2SiO3溶液与过量的CO2反应的离子方程式为______.
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
①实验①最先溶解的金属发生反应的化学方程式是______.
②滤渣B中Fe的质量分数为______%(精确到0.1%).

请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和______(填化学式).
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为______;滤渣D、稀硫酸和试剂a总反应的化学方程式为______.
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加______.
Na2SiO3溶液与过量的CO2反应的离子方程式为______.
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | ||
| NO体积(L,体积) | 1.12 | 2.24 | 3.36 | 4.48 |
②滤渣B中Fe的质量分数为______%(精确到0.1%).