摘要:将K2MnO4溶液酸化时.可制得KmnO4:3MnO42- + 4H+ = 2MnO4- + MnO2 + 2H2O .但最高产率只有66.7%.所以制取KMnO4常用电解法.即用铁.石墨作电极电解K2MnO4溶液.下列有关叙述正确的是 (A)铁作阳极.阳极的电极反应是Fe-2e=Fe2+ (B)铁作阴极.电极反应为2H+ +2e = H2↑ (C)石墨作阳极.电极反应为MnO42- - e = MnO4- (D)石墨作阳极.电极反应为4OH- - 4e = 2H2O + O2
网址:http://m.1010jiajiao.com/timu3_id_253497[举报]
将K2MnO4溶液酸化可制得KMnO4:3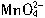 +4H+=2
+4H+=2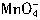 +MnO2+2H2O,但最高产率只有66.7%,所以制取KMnO4常用电解法,即以铁和石墨做电极电解K2MnO4溶液,下列有关叙述正确的是( )。
+MnO2+2H2O,但最高产率只有66.7%,所以制取KMnO4常用电解法,即以铁和石墨做电极电解K2MnO4溶液,下列有关叙述正确的是( )。
A.铁做阴极,电极反应为Fe→2Fe2++2e-
B.铁做阳极,电极反应为2H++2e-→H2↑
C.石墨做阳极,电极反应为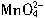 →
→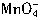 +e-
+e-
D.石墨做阴极,电极反应为4OH-→O2↑+2H2O+4e- 查看习题详情和答案>>
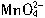 +4H+=2
+4H+=2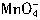 +MnO2+2H2O,但最高产率只有66.7%,所以制取KMnO4常用电解法,即以铁和石墨做电极电解K2MnO4溶液,下列有关叙述正确的是( )。
+MnO2+2H2O,但最高产率只有66.7%,所以制取KMnO4常用电解法,即以铁和石墨做电极电解K2MnO4溶液,下列有关叙述正确的是( )。A.铁做阴极,电极反应为Fe→2Fe2++2e-
B.铁做阳极,电极反应为2H++2e-→H2↑
C.石墨做阳极,电极反应为
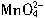 →
→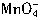 +e-
+e-D.石墨做阴极,电极反应为4OH-→O2↑+2H2O+4e- 查看习题详情和答案>>
化学实验室中常将溶液或试剂进行酸化,下列酸化处理正确的是( )
| A、为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化 | B、鉴别溶液中是否含有Br-时,所加的AgNO3溶液用硝酸酸化 | C、鉴定待测溶液中是否含有SO42-时,先用硝酸酸化,再加BaCl2溶液 | D、检验C2H5Cl中Cl元素时,将C2H5Cl和NaOH溶液混合加热后,加硫酸酸化 |
Ⅰ.一氧化碳是一种用途相当广泛的化工基础原料.
(1)利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍.
Ni(s)+4CO(g) Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H
(2)在高温下一氧化碳可将二氧化硫还原为单质硫.已知:
C(s)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1
CO2(g)+C(s)=2CO(g)△H2=+172.5kJ?mol-1
S(s)+O2(g)=SO2(g)△H3=-296.0kJ?mol-1
请写出CO除SO2的热化学方程式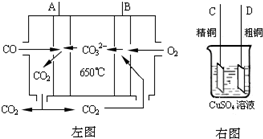
(3)如图中左图是一碳酸盐燃料电池,它以CO为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质,右图是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验.回答下列问题:
①写出A极发生的电极反应式
②要用燃料电池为电源进行粗铜的精炼实验,则B极应该与
③当消耗2.24L(标况下)CO时,粗铜电极理论上减少铜的质量
Ⅱ.(1)已知Na2CrO4溶液酸化时发生的反应为:2CrO42-+2H+?Cr2O72-+H2O,若1L酸化后所得溶液中铬元素的总物质的量为0.55mol,CrO42-有
转化为Cr2O72-.又知:常温时该反应的平衡常数K=1014.上述酸化后所得溶液的pH=
(2)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol?L-1以下才能排放.含CrO42-的废水处理通常有以下两种方法.
①沉淀法:加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+.加入可溶性钡盐后的废水中Ba2+的浓度应不小于
②还原法:CrO42-
Cr3+
Cr(OH)3.用该方法处理10m3 CrO42-的物质的量浓度为1.0×10-3 mol?L-1的废水,至少需要绿矾(FeSO4?7H2O,相对分子质量为278)
查看习题详情和答案>>
(1)利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍.
Ni(s)+4CO(g)
 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H<
<
0 (选填“>”或“=”或“<”).(2)在高温下一氧化碳可将二氧化硫还原为单质硫.已知:
C(s)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1
CO2(g)+C(s)=2CO(g)△H2=+172.5kJ?mol-1
S(s)+O2(g)=SO2(g)△H3=-296.0kJ?mol-1
请写出CO除SO2的热化学方程式
2CO(g)+SO2(g)=S(s)+2CO2(g)△H3=-270kJ?mol-1
2CO(g)+SO2(g)=S(s)+2CO2(g)△H3=-270kJ?mol-1
.
(3)如图中左图是一碳酸盐燃料电池,它以CO为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质,右图是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验.回答下列问题:
①写出A极发生的电极反应式
CO-2e-+CO32-=2CO2
CO-2e-+CO32-=2CO2
.②要用燃料电池为电源进行粗铜的精炼实验,则B极应该与
D
D
极 (填:“C”或“D”)相连.③当消耗2.24L(标况下)CO时,粗铜电极理论上减少铜的质量
小于
小于
(填:“大于”、“等于”或“小于”)6.4克.Ⅱ.(1)已知Na2CrO4溶液酸化时发生的反应为:2CrO42-+2H+?Cr2O72-+H2O,若1L酸化后所得溶液中铬元素的总物质的量为0.55mol,CrO42-有
| 10 |
| 11 |
6
6
.(2)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol?L-1以下才能排放.含CrO42-的废水处理通常有以下两种方法.
①沉淀法:加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+.加入可溶性钡盐后的废水中Ba2+的浓度应不小于
2.4×10-4
2.4×10-4
mol?L-1,然后再进行后续处理方能达到国家排放标准.②还原法:CrO42-
| ||
| 氢离子 |
| 石灰水 |
8.34
8.34
Kg(保留两位小数).