摘要:填写下列空白 化合物类别 烷烃 烯烃 炔烃 苯 结构特点 仅含碳碳单键 含有C=C 含有C≡C 碳与碳之间形成介于单.双键之间的独特的键 通式 CnH2n+2 CnH2n CnH2n-2 CnH2n-6 与溴反应类型 取代 加成 加成 取代 加入酸性高锰酸钾溶液现象 不褪色 褪色 褪色 不褪色 性质特点 易取代 易加成 易加成 易取代难加成
网址:http://m.1010jiajiao.com/timu3_id_253054[举报]
填写下列空白:
(1)34g NH3共有
(2)在标准状况下,35.5g Cl2的体积约是
(3)欲配制500mL 0.2mol/L Na2CO3溶液,需要用天平称量Na2CO3?10H2O晶体质量为
查看习题详情和答案>>
(1)34g NH3共有
8
8
mol原子,0.1molH2S共约有1.204×1023
1.204×1023
个氢原子.同温同压下,等体积的NH3和H2S气体的质量比为1:2
1:2
,含有的分子数目之比为1:1
1:1
.等质量的NH3和H2S中分子数目之比为2:1
2:1
.(2)在标准状况下,35.5g Cl2的体积约是
11.2
11.2
L,将其与氢气完全化合生成氯化氢需氢气的物质的量是0.5
0.5
mol,将生成的氯化氢气体溶于1000g水中,得到密度为a g?cm-3的盐酸,则该盐酸的物质的量浓度是(a/1.0365
1.0365
)mol/L.(3)欲配制500mL 0.2mol/L Na2CO3溶液,需要用天平称量Na2CO3?10H2O晶体质量为
28.6g
28.6g
.若从配好的上述溶液中取出50mL于一试剂瓶中,需要给它贴上标签,标签上的内容是0.2mol/L Na2CO3溶液
0.2mol/L Na2CO3溶液
;若再从中取出10mL溶液加水稀释至20mL,则此溶液中Na+的物质的量浓度为0.2mol/L
0.2mol/L
.(2006?南充一模)今有物质A及两种淡黄色的固体B和F;A、B都能与冷水反应,生成同一种物质C,同时A的反应还放出气体D,B的反应还放出气体E;D和E都能与淡黄色固体F化合,分别生成气体G和H;G和H反应又能生成固体F,固体F能溶于CS2.
试根据以上信息填写下列空白:
(1)B的电子式: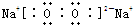
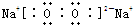 ;C物质中含有的化学键类型:
;C物质中含有的化学键类型: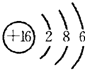
 ;
;
(2)A与水反应的离子方程式:
(3)B与H反应的化学方程式:
(4)F与C的热溶液反应的离子方程式:
查看习题详情和答案>>
试根据以上信息填写下列空白:
(1)B的电子式:
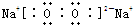
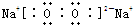
离子键和共价键
离子键和共价键
;F的原子结构示意图为

(2)A与水反应的离子方程式:
2Na+2H2O=2OH-+H2↑+2Na+
2Na+2H2O=2OH-+H2↑+2Na+
;(3)B与H反应的化学方程式:
Na2O2+SO2=Na2SO4
Na2O2+SO2=Na2SO4
;(4)F与C的热溶液反应的离子方程式:
3S+6OH-
2S2-+SO32-+3H2O
| ||
3S+6OH-
2S2-+SO32-+3H2O
.
| ||
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为地壳中含量最多的金属元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素,其中F为红褐色沉淀.四氧化三铁遇酸可能发生反应
Fe3O4+8H+=2Fe3++Fe3++4H2O
请填写下列空白:
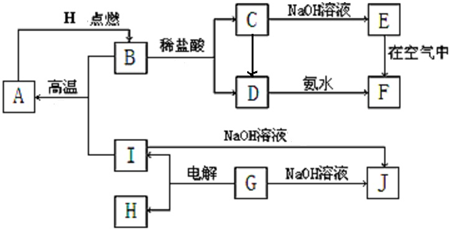
(1)若C→D为化合反应,则此时的化学方程式 ;
(2)写出G→J的离子方程式 ;
(3)写出D→F的离子方程式 .
查看习题详情和答案>>
Fe3O4+8H+=2Fe3++Fe3++4H2O
请填写下列空白:

(1)若C→D为化合反应,则此时的化学方程式
(2)写出G→J的离子方程式
(3)写出D→F的离子方程式
如图是无机物A~N在一定条件下的转化关系(部分产物及反应条件未列出).其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体.N中只含有两种元素,N可作为工业生产C的原料.
请填写下列空白:
(1)单质G: .
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是 (填写序号).
(3)反应⑩的离子方程式是 .
(4)反应④的离子方程式是 .
(5)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾).同时还生成KNO2和H2O.该反应的化学方程式是: .
(6)现有1molN参加反应,假设各步反应均完全,生成C的质量为490g,生成G的质量为224g,则反应①的化学方程式为 .
查看习题详情和答案>>

请填写下列空白:
(1)单质G:
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是
(3)反应⑩的离子方程式是
(4)反应④的离子方程式是
(5)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾).同时还生成KNO2和H2O.该反应的化学方程式是:
(6)现有1molN参加反应,假设各步反应均完全,生成C的质量为490g,生成G的质量为224g,则反应①的化学方程式为
