网址:http://m.1010jiajiao.com/timu3_id_252805[举报]
汽车的发明与使用,是人类智慧的杰出体现,它为人们的生活和生产带来了
极大的方便,同时由此引发的环境污染问题也越来越引起人们的关注,人们开始研
究新的清洁燃料.
(1)新型环保出租车采用LPG+汽油的双燃料系统,其尾气中的有毒气体成分较普
通车型下降80%左右,缓解了汽车尾气排放给城市环境造成的污染问题.下列物质
中不属于上述有害气体的是________.
A.CO2和H2 B.NO2和NO
C.CO和SO2 D.C粒和含铅化合物
(2)为了减少大气污染,许多城市推广使用汽车清洁燃料.目前使用的清洁燃料主要
有两类:一类是压缩天然气,另一类是液化石油气.这两类燃料的主要成分都是
________.
A.碳水化合物 B.碳氢化合物
C.氢气 D.醇类
(3)我国推广使用乙醇汽油,它是在汽油中加入适量乙醇形成的混合燃料.下列叙述
中正确的是________.
A.使用乙醇汽油能减少有害气体的排放,是一种改善环境的清洁能源
B.燃料中的乙醇可以通过粮食发酵或化工合成等方法制得
C.乙醇汽油是一种新型化合物
D.燃烧乙醇汽油可以减少对大气的污染是因为它不含硫元素和氮元素
(4)氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车
备受青睐.我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世
界先进水平,并加快向产业化的目标迈进.氢能具有的优点包括________.
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A.①② B.①③ C.③④ D.②④
查看习题详情和答案>>
对电动汽车和燃油汽车的比较
当前,因汽车造成的环境污染日益严重,而电动汽车却有许多优点:无污染;运行经济,每千米成本大约是汽油车辆的1/2;开起来平稳、安静、安全;维修费用低;冬天容易启动和停止。尽管有这么多的优点,目前电动汽车却难以大规模发展,其中的关键问题是什么?可能的解决方向在哪里?看过下文,你会有所了解。
(1)效率
在任何车辆中,能源所储存的能量决不会完全转化为动能,能量的一部分总是作为热消耗掉了,百分效率就给出了储存的能量转化为动能的百分比。下图为二者的能量转换百分比。
![]()
(2)能量密度
储存电需要蓄电池,储存汽油需要油箱,所谓能量密度,就是每千克储能物质所储存的能量。下图是汽油和普通汽车用蓄电池的对比。
![]()
(3)行程
车辆每充一次电或装满一箱汽油能够行驶的距离叫做它的行程。
谁都希望加一次油或充一次电行驶的距离越远越好,行程决定了车辆使用是否方便。一般情况下,电动汽车充一次电能行驶80 km,而汽车加满一次油能行驶240 km左右。
![]()
(4)充电
电动车辆里的蓄电池,每天夜里都需要充电,给它们充电由通常的电源提供,电来自发电站,所以对于蓄电池来说,实际是由发电站提供的能量。
一个12 A的插座,能够提供3 kW的电能,即3 kJ·s-1,而汽车加油站每秒能灌到油箱里1 kg汽油,其储存的能量近3×104 kJ,所以汽车加油比电池充电的速度快1万倍。为了提供和汽车加油一样快的充电速度,要用40 cm粗的电缆线才行。
思考:通过阅读本文,你认为电动汽车和燃油汽车相比,有哪些优缺点?电动汽车目前难以发展的制约点是什么?
查看习题详情和答案>>B.防止化石燃料燃烧产生的二氧化硫和汽车尾气中的氮氧化物对大气的污染是改善大气质量的重要任务
C.避免汽车尾气中的有害气体对大气的污染,目前最有效的方法是给汽车安装尾气净化装置
D.为了防止悬浮颗粒物进入大气,应该将混有悬浮颗粒物的气体通过水洗后再排放
(1)某校化学研究性学习小组的同学在技术人员的指导下,按下列流程探究不同催化剂对NH3还原NO反应的催化性能.

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).为比较不同催化剂的催化性能,需要测量并记录的数据是
(2)为避免汽车尾气中的有害气体对大气的污染,给汽车安装尾气净化装置.净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示.
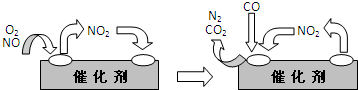
在汽车的排气管上安装“催化转化器”(用铂、钯合金作催化剂),它的作用是使CO、NO反应生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧.
①写出上述变化中的总化学反应方程式:
②用CH4催化还原NOx也可以消除氮氧化物的污染.例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H1=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H2
若1molCH4还原NO2至N2,整个过程中放出的热量为867kJ,则△H2=
(3)①有人认为:该研究可以使氨的合成反应,在铁催化剂表面进行时的效率大大提高,从而使原料的转化率大大提高.请你应用化学基本理论对此观点进行评价:
②氢气与氮气在固体催化剂表面合成氨气的反应过程可表示如下图所示,正确的顺序为
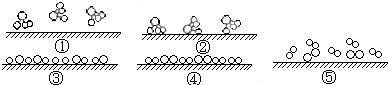
A.①②③④⑤B.②①③④⑤C.④⑤③②①D.⑤④③②①
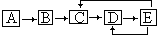
Ⅱ.A、B、C、D、E五种物质含有同一元素X,在一定条件下它们有如下转化关系,若A、B、C、D为气体且其中有一种为有色气体,E为液体,回答下列问题.
(1)B中只含两种元素,且两种元素的序数相差6,当B和E在空气中相遇时能形成大量的白烟,则D的分子式为
(2)当小心加热B与E化合时生成的物质F时,可得到一种与CO2具有相同原子数目和电子数目的气体G和另一种无色无味的液体H,写出相应的化学方程式
(1)乙丙橡胶(
 )因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是
)因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是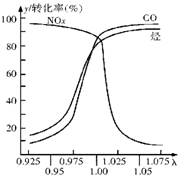
(2)在发动机和三元催化转化器间的尾气流中安装一个称为λ探测器的电化学元件,可测定λ(λ=入口处的空气量/完全燃烧需要的空气量)值,如图所示.当汽车速度增加时,入口处的空气量增大,此时排出尾气中的主要污染物是
(3)测定汽车尾气中NO,NO2的方法之一,用3%的H2O2溶液吸收生成HNO3,再用NaOH标准溶液滴定.若要确定尾气中NO,NO2体积分数总和,所需的数据有
A.气体样品的体积
B.NaOH标准溶液的浓度及所消耗的体积
C.从滴定开始到指示剂变色所需的时间
D.两种氮氧化物的体积比
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料.写出用合成气(CO和H2)生产甲醇的化学方程式