题目内容
随着经济发展和人民生活水平的提高,近年来我省汽车拥有量呈较快增长趋势.
(1)乙丙橡胶(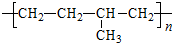 )因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是 .
)因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是 .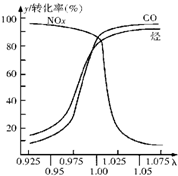
(2)在发动机和三元催化转化器间的尾气流中安装一个称为λ探测器的电化学元件,可测定λ(λ=入口处的空气量/完全燃烧需要的空气量)值,如图所示.当汽车速度增加时,入口处的空气量增大,此时排出尾气中的主要污染物是 .在转化器的前半部,一氧化碳和氮氧化物(NOx)通过催化剂发生反应转化为无污染的气体,其反应的化学方程式为 .
(3)测定汽车尾气中NO,NO2的方法之一,用3%的H2O2溶液吸收生成HNO3,再用NaOH标准溶液滴定.若要确定尾气中NO,NO2体积分数总和,所需的数据有 (选填序号).
A.气体样品的体积
B.NaOH标准溶液的浓度及所消耗的体积
C.从滴定开始到指示剂变色所需的时间
D.两种氮氧化物的体积比
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料.写出用合成气(CO和H2)生产甲醇的化学方程式 ,用该方法合成甲醇的最大优点是 .已知甲醇燃烧热为726kJ/mol.请写出甲醇燃烧的热化学方程式 .
(1)乙丙橡胶(
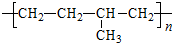 )因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是
)因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是
(2)在发动机和三元催化转化器间的尾气流中安装一个称为λ探测器的电化学元件,可测定λ(λ=入口处的空气量/完全燃烧需要的空气量)值,如图所示.当汽车速度增加时,入口处的空气量增大,此时排出尾气中的主要污染物是
(3)测定汽车尾气中NO,NO2的方法之一,用3%的H2O2溶液吸收生成HNO3,再用NaOH标准溶液滴定.若要确定尾气中NO,NO2体积分数总和,所需的数据有
A.气体样品的体积
B.NaOH标准溶液的浓度及所消耗的体积
C.从滴定开始到指示剂变色所需的时间
D.两种氮氧化物的体积比
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料.写出用合成气(CO和H2)生产甲醇的化学方程式
分析:(1)凡链节中主碳链为4个碳原子,无碳碳双键结构,其单体必为两种,从主链中间断开后,再分别将两个半键闭合即得单体;凡链节中主碳链为6个碳原子,含有碳碳双键结构,单体为两种(即单烯烃和二烯烃);
(2)汽车尾气主要污染物是氮氧化物;一氧化碳和氮氧化物(NOx)通过催化剂发生反应转化为无污染的气体氮气和二氧化碳;
(3)根据用NaOH标准溶液滴定HNO3进行解答;
(4)一氧化碳和氢气反应生成甲醇,该反应属于化合反应,原子利用率高;根据甲醇的燃烧热书写其热化学反应方程式.
(2)汽车尾气主要污染物是氮氧化物;一氧化碳和氮氧化物(NOx)通过催化剂发生反应转化为无污染的气体氮气和二氧化碳;
(3)根据用NaOH标准溶液滴定HNO3进行解答;
(4)一氧化碳和氢气反应生成甲醇,该反应属于化合反应,原子利用率高;根据甲醇的燃烧热书写其热化学反应方程式.
解答:解:(1)凡链节中主碳链为4个碳原子,无碳碳双键结构,其单体必为两种,从主链中间断开后,再分别将两个半键闭合即得单体,所以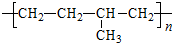 的单体是CH3-CH=CH2和CH2=CH2,
的单体是CH3-CH=CH2和CH2=CH2,
故答案为:CH3-CH=CH2和CH2=CH2;
(2)汽车尾气主要污染物是氮氧化物;一氧化碳和氮氧化物(NOx)通过催化剂发生反应转化为无污染的气体氮气和二氧化碳,反应方程式为2xCO+2NOX
N2+2xCO2,
故答案为:NOX;2xCO+2NOX
N2+2xCO2;
(3)因NOx转化为HNO3后再用NaOH标准溶液滴定,由N元素守恒知n(NOx)=n(HNO3),所以要测尾气中NOx的体积分数,需要测定尾气的总体积、滴定消耗的NaOH标准溶液的体积及其物质的量浓度,
故选:AB;
(4)一氧化碳和氢气反应生成甲醇,反应方程式为CO+2H2═CH3OH,该反应属于化合反应,没有副产物生成,所以原子利用率100%,甲醇燃烧热为726kJ/mol,则2mol甲醇完全燃烧放出1452kJ热量,则其热化学反应方程式为2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol,
故答案为:CO+2H2═CH3OH;原子利用率为100%;2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol.
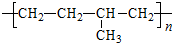 的单体是CH3-CH=CH2和CH2=CH2,
的单体是CH3-CH=CH2和CH2=CH2,故答案为:CH3-CH=CH2和CH2=CH2;
(2)汽车尾气主要污染物是氮氧化物;一氧化碳和氮氧化物(NOx)通过催化剂发生反应转化为无污染的气体氮气和二氧化碳,反应方程式为2xCO+2NOX
| ||
故答案为:NOX;2xCO+2NOX
| ||
(3)因NOx转化为HNO3后再用NaOH标准溶液滴定,由N元素守恒知n(NOx)=n(HNO3),所以要测尾气中NOx的体积分数,需要测定尾气的总体积、滴定消耗的NaOH标准溶液的体积及其物质的量浓度,
故选:AB;
(4)一氧化碳和氢气反应生成甲醇,反应方程式为CO+2H2═CH3OH,该反应属于化合反应,没有副产物生成,所以原子利用率100%,甲醇燃烧热为726kJ/mol,则2mol甲醇完全燃烧放出1452kJ热量,则其热化学反应方程式为2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol,
故答案为:CO+2H2═CH3OH;原子利用率为100%;2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol.
点评:本题考查了氮及其化合物对环境的影响、有机物单体的确定等知识点,难点是有机物单体的判断、酸碱中和滴定实验,难度中等.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
 (2010?聊城一模)随着经济发展现在汽车越来越多,同时也带来了交通拥挤和空气污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
(2010?聊城一模)随着经济发展现在汽车越来越多,同时也带来了交通拥挤和空气污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
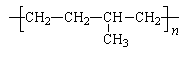 )因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是 。
)因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是 。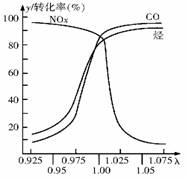

 CO+N2
CO+N2