摘要:14.下列溶液中.c(H+)最大的是 A.0.1 mol/L HCl溶液 B.0.1 mol/L NaOH溶液 C.0.1 mol/L H2SO4溶液 D.0.1 mol/L CH3COOH溶液
网址:http://m.1010jiajiao.com/timu3_id_250968[举报]
|
下列溶液中,c(H+)最大的是 | |
| [ ] | |
A. |
0.1 mol·L-1 HCl溶液 |
B. |
0.1 mol·L-1 H2SO4溶液 |
C. |
0.1 mol·L-1 NaOH溶液 |
D. |
0.1 mol·L-1 CH3COOH溶液 |
有①Na2SO3溶液②CH3COOH溶液③HCl溶液各25 mL,物质的量浓度均为0.1 mol/L。下列说法正确的是( )
| A.三种溶液的pH的大小顺序是①﹥②﹥③ |
| B.三种溶液稀释相同倍数,pH变化最大的是① |
| C.三种溶液中含微粒种类多少顺序是:②﹥①﹥③ |
| D.三种溶液中由水电离出c(H+)大小顺序是:③﹥②﹥① |
有①Na2SO3溶液②CH3COOH溶液③HCl溶液各25 mL,物质的量浓度均为0.1 mol/L。下列说法正确的是( )
| A.三种溶液的pH的大小顺序是①﹥②﹥③ |
| B.三种溶液稀释相同倍数,pH变化最大的是① |
| C.三种溶液中含微粒种类多少顺序是:②﹥①﹥③ |
| D.三种溶液中由水电离出c(H+)大小顺序是:③﹥②﹥① |
现有常温下的四份溶液:①0.01 mol·L-1 CH3COOH;②0.01 mol·L-1 HCl;③pH=12的氨水;④pH=12的NaOH溶液。下列说法正确的是
A.①中水的电离程度最小,③中水的电离程度最大
B.将②③混合,若有pH=7,则消耗溶液的体积:②>③
C.将四份溶液稀释相同倍数后,溶液的pH:③>④,②>①
D.将①④混合,若有c(CH3COO-)>c(H+),则混合液一定呈碱性
查看习题详情和答案>>常温下,在10 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是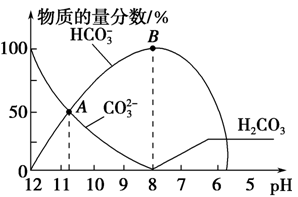
| A.在0.1 mol·L-1 Na2CO3溶液中:c(Na+)+ c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| B.当溶液的pH为7时,溶液的总体积为20 ml |
| C.在B点所示的溶液中,浓度最大的阳离子是Na+ |
| D.在A点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-) |