摘要:3.2003-5-12号河南电视台报道:某过氧乙酸消毒剂制备厂.装运过氧化氢的卡车突然发生爆炸.造成5人受伤.下面是各“行家 的分析.你认为正确的是 ( ) A.过氧化氢振动.产生了大量可燃性气体.遇明火发生爆炸. B.过氧化氢分解.产生高浓度氧气.遇某些易燃物在明火作用下而发生爆炸 C.可能是某工人在附近吸烟引起过氧化氢爆炸. D.可能是工厂的冰醋酸蒸气与过氧化氢蒸气相遇发生爆炸. 第28届国际地质大会提供的资料显示.海底有大量的天然气水合物.可满足人类 1000年的能源需要.天然气水合物是一种晶体.晶体中平均每46个水分子构建成8个笼.每个笼可容纳五个CH4分子或1个游离H2O分子. 根据上述信息.完成第4.5题.
网址:http://m.1010jiajiao.com/timu3_id_249760[举报]
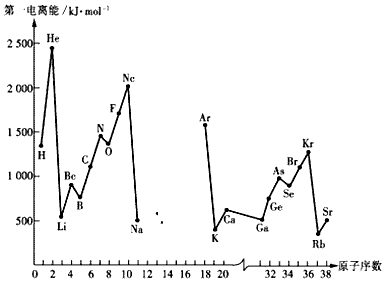
第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
请回答以下问题
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na--Ar元素中,Al的第一电离能的大小(最小)范围为________<Al<_________(填元素符号)。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是______________;
(3)上图中第一电离能最小的元素在周期表中的位置是________________________;
(4)根据对角线规则,Be、Al元素最高氧化物水化物的性质相似,它们都具有__________性,其中
Be(OH)2显示这种性质的离子方程式是:________________________、_______________________。
(5)单质C不可能具有的性质是___________
A.具有良好的导电性
B.熔沸点很高
C.硬度较小
D.易与Br单质反应,形成的化合物分子是极性分子
查看习题详情和答案>>
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na--Ar元素中,Al的第一电离能的大小(最小)范围为________<Al<_________(填元素符号)。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是______________;
(3)上图中第一电离能最小的元素在周期表中的位置是________________________;
(4)根据对角线规则,Be、Al元素最高氧化物水化物的性质相似,它们都具有__________性,其中
Be(OH)2显示这种性质的离子方程式是:________________________、_______________________。
(5)单质C不可能具有的性质是___________
A.具有良好的导电性
B.熔沸点很高
C.硬度较小
D.易与Br单质反应,形成的化合物分子是极性分子
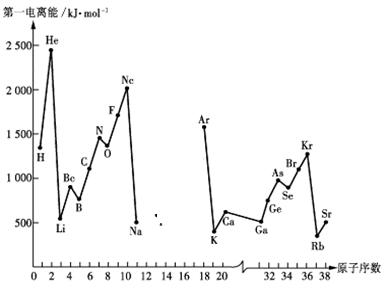
第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na——Ar元素中,Al的第一电离能的大小(最小)范围为 <Al< (填元素符号)。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是______________;
(3)上图中第一电离能最小的元素在周期表中的位置是________________________;
(4)根据对角线规则,Be、Al元素最高氧化物水化物的性质相似,它们都具有 性,其中Be(OH)2显示这种性质的离子方程式是:________________________ ___、______________________________________。
(5)单质C不可能具有的性质是
A.具有良好的导电性
B.熔沸点很高
C.硬度较小
D.易与Br单质反应,形成的化合物分子是极性分子。
查看习题详情和答案>>用a、b两个质量相等的Pt电极电解AlCl3和CuSO4混合溶液,已知溶液中n(AlCl3):n(CuSO4)=1:12,
t1时刻a电极得到混合气体,其中Cl2在标准状况下为224mL(忽略气体的溶解);t2时刻Cu全部在电极上析出.下列判断正确的是( )
t1时刻a电极得到混合气体,其中Cl2在标准状况下为224mL(忽略气体的溶解);t2时刻Cu全部在电极上析出.下列判断正确的是( )
查看习题详情和答案>>
 第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失).
第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失).请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小(最小)范围为
Na
Na
<Al<Mg
Mg
(填元素符号).(2)从图分析可知,同一主族元素原子的第一电离能I1变化规律是
从上到下依次减小
从上到下依次减小
.(3)图中第一电离能最小的元素在周期表中的位置是
第五周期ⅠA族
第五周期ⅠA族
.(4)根据对角线规则,Be、Al元素最高氧化物的水化物性质相似,它们都具有
两性
两性
,其中Be(OH)2显示这种性质的离子方程式是Be(OH)2+2H+=Be2++2H2O
Be(OH)2+2H+=Be2++2H2O
、Be(OH)2+2OH-=BeO2-+2H2O
Be(OH)2+2OH-=BeO2-+2H2O
.