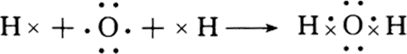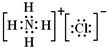摘要:24用电子式表示下列化合物的形成过程: (1)CH4 (2)MgCl2 25在NaCl.NaOH.N2.H2S中.只含有离子键的是 .只含有极性键的是 .只含有非极性键的是 .既含有离子键又有极性键的是 .26.下列实验操作中错误的是 . A.蒸发操作时.待蒸发皿中的水分完全蒸干后再停止加热 B.将饱和FeCl3溶液滴入沸水中制取Fe(OH)3胶体 C.蒸馏和测定中和反应反应热时.温度计水银球均需浸没在液体中 D.分液操作时.分液漏斗中下层液体从下口放出.上层液体从上口倒出 E.选用酒精作为萃取剂从碘水中萃取碘. F.把氢氧化钠固体放在托盘天平左盘的滤纸上称量 G.用酒精灯的外焰给试管中的物质加热 H.过滤操作中.为了加快过滤可用玻璃棒在漏斗中轻轻搅拌 27利用氧化还原反应2FeCl3+Cu=2FeCl2+CuCl2.设计一个原电池装置.要求: ⑴ 画出装置图.标明电极材料和电解质溶液, ⑵ 写出电极反应式. 28.取含MnO2的软锰矿17.4g与足量浓HCl反应后.将生成的Cl2通入含22g NaBr的水溶液中.经加热蒸发水分并烘干后.得质量为13.1g的残渣.计算: (1)生成 NaCl多少克? (2)生成Cl2多少克? (3)软锰矿含MnO2的质量分数.
网址:http://m.1010jiajiao.com/timu3_id_249705[举报]
A、B、C、D、E、F六种短周期元素的原子序数依次增大,已知:①A原子核内只有1个质子;②B原子最外层电子数是次外层电子数的2倍;③C原子最外层电子数比次外层电子数多4个;④D原子的次外层电子数是最外层电子数的8倍;⑤E单质既能和盐酸反应又能和烧碱反应;⑥F与C同主族.用化学符号或化学用语回答下列问题:
(1)用电子式表示下列物质A2C2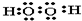
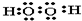 ,DCA
,DCA
 ;
;
(2)用电子式表示D与F形成化合物的过程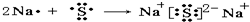
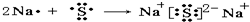 ;
;
(3)用“化学式”和“<或>”比较:A与C、A与F形成化合物的稳定性
(4)写出E与烧碱反应的离子方程式
查看习题详情和答案>>
(1)用电子式表示下列物质A2C2
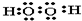
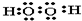


(2)用电子式表示D与F形成化合物的过程
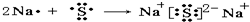
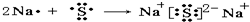
(3)用“化学式”和“<或>”比较:A与C、A与F形成化合物的稳定性
H2O>H2S
H2O>H2S
;沸点的高低H2O>H2S
H2O>H2S
,沸点高低的原因H2O分子间存在氢键
H2O分子间存在氢键
;(4)写出E与烧碱反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.