摘要:在温热条件下.萘()可用浓硝酸和浓硫酸的混酸进行硝化.生成的硝基一元取代物有 1种 B. 2种 C. 3种 D. 4种
网址:http://m.1010jiajiao.com/timu3_id_249571[举报]
煤焦油的成分主要是酚类和萘。萘的分子式是C10H8,结构简式是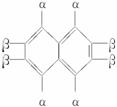 。在30—
。在30—60 ℃ 条件下,萘可用浓HNO3和浓H2SO4的混酸进行硝化,生成的一硝基取代物有( )
A.1种 B.2种 C.3种 D.4种
查看习题详情和答案>>从含银、铜、金和铂的金属废料中提取金、银、铂的一种工艺如下:

根据以上工艺回答下列问题:
(1)电解时,以
(2)AgCl溶于氨水后所得的溶液含有的一种阳离子,在碱性条件下,也可用葡萄糖将其还原为银,写出该反应的离子方程式:
(3)写出步骤(4)的离子反应方程式:
(4)王水是
(5)金和浓硝酸反应的化学方程式为:Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O
但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释之:
查看习题详情和答案>>

根据以上工艺回答下列问题:
(1)电解时,以
金属废料
金属废料
为阳极,纯铜为阴极,CuSO4溶液为电解液,则阳极的电极反应式为:Cu-2e-→Cu2+
Cu-2e-→Cu2+
(2)AgCl溶于氨水后所得的溶液含有的一种阳离子,在碱性条件下,也可用葡萄糖将其还原为银,写出该反应的离子方程式:
2[Ag(NH3)2]++2OH-+CH2OH(CHOH)4CHO 2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
 2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
2Ag+4NH3+CH2OH(CHOH)4COOH+H2O2[Ag(NH3)2]++2OH-+CH2OH(CHOH)4CHO 2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
; 2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
2Ag+4NH3+CH2OH(CHOH)4COOH+H2O(3)写出步骤(4)的离子反应方程式:
2AuCl4-+3SO2+6H2O=2Au+8Cl-+3SO42-+12H+
2AuCl4-+3SO2+6H2O=2Au+8Cl-+3SO42-+12H+
;(4)王水是
浓盐酸和浓硝酸
浓盐酸和浓硝酸
的混合液,其体积比为:3:1
3:1
(5)金和浓硝酸反应的化学方程式为:Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O
但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释之:
王水中含有大量的Cl-,Au3+与Cl-可生成AuCl4-,使该平衡中Au3+浓度降低,平衡正移,金即可溶于王水
王水中含有大量的Cl-,Au3+与Cl-可生成AuCl4-,使该平衡中Au3+浓度降低,平衡正移,金即可溶于王水
.在一定条件下,萘可以被硝硫混酸硝化生成二硝基物,它是1.5-二硝基萘( )和1.8-二硝基萘(
)和1.8-二硝基萘( )的混合物.后者可溶于质量分数大于98%的硫酸,而前者不能.利用这个性质可以将这两种异构体分离.将上述硝化产物放入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1.8-二硝基萘,应彩的方法是( )
)的混合物.后者可溶于质量分数大于98%的硫酸,而前者不能.利用这个性质可以将这两种异构体分离.将上述硝化产物放入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1.8-二硝基萘,应彩的方法是( )
 )和1.8-二硝基萘(
)和1.8-二硝基萘( )的混合物.后者可溶于质量分数大于98%的硫酸,而前者不能.利用这个性质可以将这两种异构体分离.将上述硝化产物放入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1.8-二硝基萘,应彩的方法是( )
)的混合物.后者可溶于质量分数大于98%的硫酸,而前者不能.利用这个性质可以将这两种异构体分离.将上述硝化产物放入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1.8-二硝基萘,应彩的方法是( )
查看习题详情和答案>>