摘要:2005年12月吉林石化公司双苯厂苯胺装置硝化单元发生着火爆炸.引起松花江流域大面积的水污染.居民的饮用水一度处于紧张状态.已知苯胺可由硝基苯经下列反应而得到.+3Fe+6HCl→+3FeCl2+2H2O.下列有关说法正确的是 A.由硝基苯生成苯胺.硝基苯被还原 B.由硝基苯生成苯胺.硝基苯被氧化 C.该反应的还原剂是Fe.每生成1mol苯胺转移4mol电子 D.该反应中的还原剂是HCl.每生成1mol苯胺转移2mol电子
网址:http://m.1010jiajiao.com/timu3_id_248735[举报]
《光明日报》报道,我国首个以海水为能源的空调示范项目2005年在华电青岛发电有限公司已经获得成功。2005年11月吉林石化公司双苯厂苯胺装置硝化单元发生着火爆炸,引起松花江大面积的水污染,居民的饮用水一度处于紧张状态。下列关于水的说法中错误的是( )
A.用膜分离的方法可以使海水淡化。
B.高效催化剂可使水分解,同时释放出能量
C.氯气、漂白精[主要成分是Ca(ClO)2]、活性炭是常见的水处理剂,但它们处理水的原理并不完全相同
D.固态冰的密度小于液态水的密度与水分子间可以形成氢键有关
查看习题详情和答案>>《光明日报》报道,我国首个以海水为能源的空调示范项目2005年在华电青岛发电有限公司已获得成功。2005年11月吉林石化公司双苯厂苯胺装置化单元发生着火爆炸,引起松花江大面积的水污染,居民的饮用水一度处于紧张状态。下列关于水的说法中错误的是 ( )
A.用膜分离的方法可以使海水淡化
B.高效催化剂可使水分解,同时释放出能量
C.氯气、漂白精[主要成分是Ca(C1O)2]、活性炭是常见的水处理剂,但它们处理水的原理并不完全相同
D.固态冰的密度小于液态水的密度与水分子间以形成氢键有关
查看习题详情和答案>>2005年12月12日中央电视台等媒体报道,市场上的膨化食品中有三成以上铝严重超标,长期食用铝含量过高的膨化食品,会干扰人的思维、意识和记忆功能,引起神经系统病变,严重者可能痴呆.下列有关说法正确的是( )
查看习题详情和答案>>
(2009?广州二模)水是生命之源,2005年12月发生在我省的北江水污染事件再次提醒人们保护水资源的必要性和紧迫性.
(1)据报道,北江水污染事件是由于某冶炼厂设备检修期间排放的废水所致,推测其主要污染物是
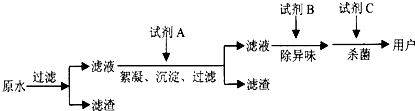
(2)自来水的生产流程如图,其中的试剂A、B、C分别可以选择
(3)电镀厂排放的废水中含铬(以Cr2O72-形式存在),常用电解的方法处理.电解时,以铁为阳极,生成的Fe2+将Cr2O72-还原为Cr3+,产物再与电解时生成的OH-形成氢氧化物沉淀而除去.
①两个电极上发生的反应分别为:阳极
②溶液中发生的总反应为(用离子方程式表示)
(4)化学需氧量(COD)是水体质量的控制项目这一,它是量废水中还原性污染物的重要指标.COD是指用强氧化剂(我国采用K2Cr2O7)处理一定量水样时消耗的氧化剂的量,并换算成以O2作为氧化剂时,1L水样所消耗O2的质量(mg?L-1).现取某池塘水样20.00mL,反应消耗10.00mL0.0400mol?L-1K2Cr2O7溶液(反应后转化为Cr3+).该水样的COD为
查看习题详情和答案>>
(1)据报道,北江水污染事件是由于某冶炼厂设备检修期间排放的废水所致,推测其主要污染物是
重金属离子
重金属离子
.如果有害废水已经在河流中扩散,为了尽量减少危害,对河水的处理应该采取的措施是利用上游水源稀释
利用上游水源稀释
(2)自来水的生产流程如图,其中的试剂A、B、C分别可以选择
明矾(或硫酸铁等)
明矾(或硫酸铁等)
、活性炭
活性炭
、Cl2(或ClO2、O3等)
Cl2(或ClO2、O3等)
.
(3)电镀厂排放的废水中含铬(以Cr2O72-形式存在),常用电解的方法处理.电解时,以铁为阳极,生成的Fe2+将Cr2O72-还原为Cr3+,产物再与电解时生成的OH-形成氢氧化物沉淀而除去.
①两个电极上发生的反应分别为:阳极
Fe-2e-=Fe2+
Fe-2e-=Fe2+
,阴极2H++2e-=H2↑
2H++2e-=H2↑
.②溶液中发生的总反应为(用离子方程式表示)
6Fe2++Cr2O72-+10 OH-+7H2O=6Fe(OH)3↓+2Cr(OH)3↓
6Fe2++Cr2O72-+10 OH-+7H2O=6Fe(OH)3↓+2Cr(OH)3↓
.(4)化学需氧量(COD)是水体质量的控制项目这一,它是量废水中还原性污染物的重要指标.COD是指用强氧化剂(我国采用K2Cr2O7)处理一定量水样时消耗的氧化剂的量,并换算成以O2作为氧化剂时,1L水样所消耗O2的质量(mg?L-1).现取某池塘水样20.00mL,反应消耗10.00mL0.0400mol?L-1K2Cr2O7溶液(反应后转化为Cr3+).该水样的COD为
960
960
mg?L-1.2005年12月2日新浪网报道,我国独立研制的具有自主知识产权的“龙芯2D”12月底完成流片.“龙芯2D”的面世,意味着中国在半导体产业上已取得了长足进步,同时将有着良好的发展前景.试回答下列问题:
(1)“龙芯”(芯片)的主要成分是单晶硅,硅位于元素周期表中第
(2)硅在一定条件下可以与氯气反应生成SiCl4,与氧气反应生成SiO2.四氯化硅结构中,所有原子最外层
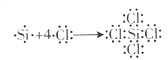
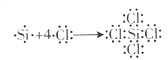 .
.
(3)试判断SiCl4的沸点比CCl4的
(4)现在新开发出一种具有和“龙芯”主要成分一样的六角形笼状结构单质分子Si12,它可能在未来的量子计算机中是一个理想的贮存信息的材料,是种六角形笼状结构:它与单晶硅互称为
查看习题详情和答案>>
(1)“龙芯”(芯片)的主要成分是单晶硅,硅位于元素周期表中第
3
3
周期ⅣA
ⅣA
族;(2)硅在一定条件下可以与氯气反应生成SiCl4,与氧气反应生成SiO2.四氯化硅结构中,所有原子最外层
是
是
(填“是、否”)都满足8电子稳定结构.用电子式表示四氯化硅的形成过程: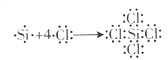
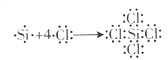
(3)试判断SiCl4的沸点比CCl4的
高
高
(填“高或低”),理由SiCl4的相对分子质量比CCl4的大,范德华力大,因此沸点高.
SiCl4的相对分子质量比CCl4的大,范德华力大,因此沸点高.
(4)现在新开发出一种具有和“龙芯”主要成分一样的六角形笼状结构单质分子Si12,它可能在未来的量子计算机中是一个理想的贮存信息的材料,是种六角形笼状结构:它与单晶硅互称为
同素异形体
同素异形体
,硅原子之间是通过共价
共价
键结合的.