网址:http://m.1010jiajiao.com/timu3_id_248268[举报]
氮元素是生命活动、物质间转化的常见元素。
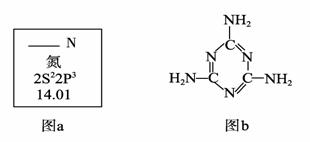
(1)图a是元素周期表中N元素的有关信息,图a中横线上缺失的具体内容是 。
15N是N元素的一种重要核素,其一个原子核中含有的中子数为 。
(2)三聚氰胺的结构简式如上图b,根据你的了解,下列关于三聚氰胺的表述中,
正确的是 (填字母序号)。
A.三聚氰胺的熔点可能很高 B.三聚氰胺的含氮量高达67%左右
C.三聚氰胺属于无机化合物 D.三聚氰胺分子中所有原子在同一平面上
(3)①最近科学家们合成了由氮元素形成的N5n+,电子式![]() 为
为
则n值为 。
②H与N能形成化合物NH5 ,已知该物质与水反应有H2生成,则NH5中含有的化学键为 。
(4)已知M为氮元素与一种金属元素组成的离子化合物,其中金属元素的质量分数为
35.4%,M在汽车安全气囊中有重要的作用。常温下G为淡黄色固体。H为一种常见的液体,A、B、C、X为单质,其中A、C、X为气体,A、X均为空气中成分。I、J为常见的工业原料。

①写出D与X反应的化学方程式
②写出G与H反应的离子方程式 。
③实验室中I应如何保存? 。
④常温下M受撞击时可分解,13gM完全分解为A和B时,放出akJ的热量,写出M分解的热化学方程式 。
⑤M是一种易溶于水的盐,其水溶液显弱碱性,用离子方程式解释原因 。
查看习题详情和答案>>验证某有机物属于烃,应完成的实验内容是
[ ]
A.只测定它的C、H之比
B.只要证明它完全燃烧后产物只有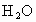 和
和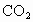
C.只测定其燃烧产物中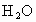 与
与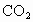 的物质的量的比值
的物质的量的比值
D.测定该试样的质量及试样完全燃烧后生成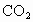 和
和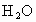 的质量
的质量
|
验证某有机物属于烃,至少应完成的实验内容是 | |
| [ ] | |
A. |
测定它的C、H比 |
B. |
证明它完全燃烧后产物只有H2O和CO2 |
C. |
测定其燃烧产物中H2O与CO2的物质的量的比值 |
D. |
测定该试样的质量及试样完全燃烧后生成CO2和H2O的质量 |

铁架台等装置略去。请你帮助他们完成下列实验报告。
(1)实验目的:_____________________。
(2)实验用品:仪器、天平、分液漏斗、锥形瓶、硬质玻璃管、干燥瓶、酒精灯、洗气瓶等.
药品:红褐色铜粉(含炭)样品,过氧化氢溶液、二氧化锰、碱石灰、浓硫酸等.
(3)实验内容:

(4)计算:样品中铜的质量分数=____________(用含W、m1、m2的代数式表示).
(5)问题和讨论:
实验完成后,老师评议说:按上述实验设计,即使G中反应完全,D中吸收完全,也不会得到正确的结果.经讨论有同学提出在B与G之间加入一个装置.再次实验后,得到了较正确的结果.那么,原来实验所测得的铜的质量分数偏小的原因可能是_____________
________.在B与G之间加入的装置可以是_________________,其中盛放的药品是_________________.
查看习题详情和答案>>