摘要:27. (1) A (2) A (3) H (4) B (5) E (6) C , F (7) F
网址:http://m.1010jiajiao.com/timu3_id_248106[举报]
A~H等8种物质存在如下转化关系(反应条件,部分产物未标出)。已知:A是正盐, B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题:
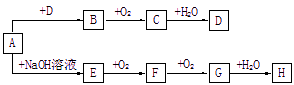
(1)写出下列物质的化学式:A ,B ,C 。
(2)写出下列反应的化学方程式:
E→F ;
G→H ;
D的浓溶液与木炭反应的方程式: 。
(3)检验某溶液中是否含D中阴离子的方法是 。
查看习题详情和答案>>A~H等8种物质存在如下转化关系(反应条件,部分产物未标出)。已知:A是正盐, B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题: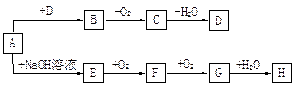
(1)写出下列物质的化学式:A ,B ,C 。
(2)写出下列反应的化学方程式:
E→F ;
G→H ;
D的浓溶液与木炭反应的方程式: 。
(3)检验某溶液中是否含D中阴离子的方法是 。
A、B、C、D、E、F六种元素,其中A、B、C、D、E为短周期主族元素.它们之间的关系如下:
Ⅰ.原子半径:A<C<B<E<D
Ⅱ.原子的最外层电子数:A=D C=E A+B=C
Ⅲ.原子的核外电子层数:B=C=2A
Ⅳ.B元素的主要化合价:最高正价+最低负价=2
请回答:
(1)甲为由A、B两种元素组成的常见气体,写出其电子式
 ;乙为由B元素组成的单质,写出该单质的一种用途
;乙为由B元素组成的单质,写出该单质的一种用途
(2)写出某黑色含F的磁性氧化物在E的最高价氧化物对应水化物的稀溶液中反应的离子方程式:
(3)向A、B、C三种元素组成的某盐溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为
(4)写出C和D形成的化合物与EC2发生氧化还原反应的化学方程式,并标出电子转移的方向和数目:
 .
.
(5)上述元素中的五种元素可形成一种常见复盐,经检测该复盐中三种离子的个数比为2:1:2.则该复盐的化学式为
查看习题详情和答案>>
Ⅰ.原子半径:A<C<B<E<D
Ⅱ.原子的最外层电子数:A=D C=E A+B=C
Ⅲ.原子的核外电子层数:B=C=2A
Ⅳ.B元素的主要化合价:最高正价+最低负价=2
请回答:
(1)甲为由A、B两种元素组成的常见气体,写出其电子式


作保护气
作保护气
.(2)写出某黑色含F的磁性氧化物在E的最高价氧化物对应水化物的稀溶液中反应的离子方程式:
Fe3O4+8H+═2Fe3++Fe2++4H2O
Fe3O4+8H+═2Fe3++Fe2++4H2O
(3)向A、B、C三种元素组成的某盐溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为
NH4NO2+AgNO3═AgNO2↓+NH4NO3
NH4NO2+AgNO3═AgNO2↓+NH4NO3
,已知该盐溶液常温下呈酸性,则0.1mol/L该盐溶液中离子浓度的大小顺序为C(NO2->C(NH4+)>C(H+)>C(OH-)
C(NO2->C(NH4+)>C(H+)>C(OH-)
(4)写出C和D形成的化合物与EC2发生氧化还原反应的化学方程式,并标出电子转移的方向和数目:


(5)上述元素中的五种元素可形成一种常见复盐,经检测该复盐中三种离子的个数比为2:1:2.则该复盐的化学式为
(NH4)2Fe(SO4)2
(NH4)2Fe(SO4)2
.为探究该复盐中的某种离子,取少量该复盐于试管中并加水溶解,滴加铁氰化钾溶液(K3[Fe(CN)6]),则现象和结论为出现蓝色沉淀,证明有Fe2+
出现蓝色沉淀,证明有Fe2+
.A、B、C、D、E、F六种短周期主族元素,原子序数依次增大.
则:
(1)B的原子结构示意图为
 .
.
(2)B、C、E分别与A形成的化合物中最稳定的是
(3)C与D形成的化合物的化学式是
(4)F的单质在反应中常作
查看习题详情和答案>>
| 元素 | 信息 |
| B | 其单质在常温下为双原子分子,与A可形成分子X,X的水溶液呈碱性 |
| D | 其简单阳离子与X具有相同电子数,且是同周期中简单阳离子中半径最小的 |
| E | 元素原子最外层比次外层少2个电子 |
| C、F | 两种元素的原子最外层共有13个电子 |
(1)B的原子结构示意图为


(2)B、C、E分别与A形成的化合物中最稳定的是
H2O
H2O
(写化学式).(3)C与D形成的化合物的化学式是
Al2O3
Al2O3
,它的性质决定了它在物质的分类中应属于两性氧化物
两性氧化物
;请写出该化合物对应水化物电离的方程式Al3++3OH-?Al(OH)3?AlO2-+H++H2O
Al3++3OH-?Al(OH)3?AlO2-+H++H2O
.(4)F的单质在反应中常作
氧化
氧化
剂,该单质的水溶液与E的低价氧化物反应的离子方程式为Cl2+SO2+2H2O═4H++2Cl-+SO4 2-
Cl2+SO2+2H2O═4H++2Cl-+SO4 2-
.A、B、C、D、E、F、G、H、I、J分别代表十种不同的有机物(其中A是化学工业重要原料之一).它们之间的相互转化关系如图: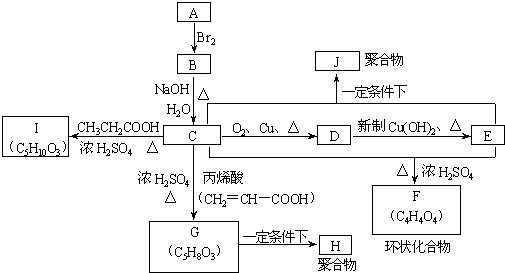
请回答下列问题:
(1)A的结构式简为
 ;指G→H的反应类型
;指G→H的反应类型
(2)写出下列转化的化学方程式.
①C→I
②C+E→J
(3)G有多种同分异构体,其中能与NaOH溶液及硫酸溶液均可反应;能发生银镜反应且生成的银与相应有机物的物质的量比为4:1,由符合条件的同分异构体数目有
查看习题详情和答案>>

请回答下列问题:
(1)A的结构式简为
CH2=CH2
CH2=CH2
;F的结构简式为

加聚反应
加聚反应
.(2)写出下列转化的化学方程式.
①C→I
CH3CH2COOH+HOCH2CH2OH
CH3CH2COOCH2CH2OH+H2O
| 浓硫酸 |
| △ |
CH3CH2COOH+HOCH2CH2OH
CH3CH2COOCH2CH2OH+H2O
| 浓硫酸 |
| △ |
②C+E→J
nCH2OHCH2CH2OH+nHOOCCOOH
 +(2n-1)H2O
+(2n-1)H2O
| 催化剂 |
 +(2n-1)H2O
+(2n-1)H2OnCH2OHCH2CH2OH+nHOOCCOOH
 +(2n-1)H2O
+(2n-1)H2O
| 催化剂 |
 +(2n-1)H2O
+(2n-1)H2O(3)G有多种同分异构体,其中能与NaOH溶液及硫酸溶液均可反应;能发生银镜反应且生成的银与相应有机物的物质的量比为4:1,由符合条件的同分异构体数目有
5
5
种,写出其中的一种同分异构体结构简式HCOOCH2CH2CH2CHO
HCOOCH2CH2CH2CHO
.