摘要:26.某不纯的K2CO3样品中含有碳酸钠.硝酸钾和氯化钡三种杂质中的一种或几种.将13.8g 样品溶于足量水中得到澄清溶液.再加入过量氯化钙溶液.得到9g沉淀.样品的组成可能是⑴ ⑵ ⑶ .
网址:http://m.1010jiajiao.com/timu3_id_24755[举报]
有如图实验装置:

(1)写出用字母标出的仪器的名称:
(2)⑤处的作用是
(3)③处的实验现象是
(4)写出①中发生的反应的化学方程式
(5)若某个同学利用该装置进行实验时,没有用②装置(硬质玻璃管+木炭),发现氧化铜粉末变红,澄清石灰水变浑浊,⑤处气体可点燃,则①装置中的固体物质除大理石外,还有可能加入了
(6)若用原实验装置测定某不纯的氧化铜样品中含铜的质量分数.(杂质不参加反应).硬质玻璃管的质量为a,充分反应记录其他实验数据如下.
根据以上数据,写出求解样品中铜的质量分数的表达式.
查看习题详情和答案>>

(1)写出用字母标出的仪器的名称:
(2)⑤处的作用是
除去未反应的CO,以免污染空气
除去未反应的CO,以免污染空气
;(3)③处的实验现象是
黑色粉末逐渐变红
黑色粉末逐渐变红
;(4)写出①中发生的反应的化学方程式
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
;(5)若某个同学利用该装置进行实验时,没有用②装置(硬质玻璃管+木炭),发现氧化铜粉末变红,澄清石灰水变浑浊,⑤处气体可点燃,则①装置中的固体物质除大理石外,还有可能加入了
锌或铁或镁或铝等
锌或铁或镁或铝等
;(6)若用原实验装置测定某不纯的氧化铜样品中含铜的质量分数.(杂质不参加反应).硬质玻璃管的质量为a,充分反应记录其他实验数据如下.
| 反应前 | 充分反应后 | |
| 硬质玻璃管③+样品的质量 | Ml | M2 |
某不纯的氯化铵样品中,测得其中氮元素的质量分数为28%,则混入的一种杂质可能是
①NH4HCO3 ②(NH4)2SO4 ③NH4NO3 ④CO(NH2)2( )
①NH4HCO3 ②(NH4)2SO4 ③NH4NO3 ④CO(NH2)2( )
| A、①或② | B、①或③ | C、②或④ | D、③或④ |
小明在研究性学习中了解到氢气具有还原性.他设计了一个实验,利用氢气的还原性来探究某不纯的氧化铜样品中氧化铜的质量分数(杂质为铜,不与氢气反应),C装置中发生反应的化学方程式为:CuO+H2
Cu+H2O
(提示:氯化钙固体可用作干燥剂,装置图如下图所示,部分起固定作用的装置未画出.)
为测定该氧化铜样品中氧化铜的质量分数,请回答问题.
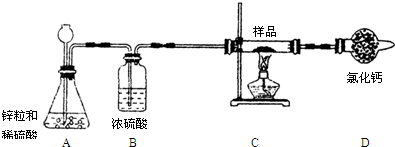
(1)第一小组设计如下实验方案:称取10g样品,放在上图所示装置的玻璃管中,使其充分反应,测得D装置质量增加了1.8g,则该样品中氧化铜的质量分数为
(2)在第一小组设计的方案中,如果将B装置删去,对测定的结果(填“有”或“无”)
(3)第二小组设计的方案:称取10g样品,放入足量的稀硫酸中,欲计算该样品中氧化铜的质量分数,还需测定的一种数据是
查看习题详情和答案>>
| ||
(提示:氯化钙固体可用作干燥剂,装置图如下图所示,部分起固定作用的装置未画出.)
为测定该氧化铜样品中氧化铜的质量分数,请回答问题.

(1)第一小组设计如下实验方案:称取10g样品,放在上图所示装置的玻璃管中,使其充分反应,测得D装置质量增加了1.8g,则该样品中氧化铜的质量分数为
80%
80%
.(2)在第一小组设计的方案中,如果将B装置删去,对测定的结果(填“有”或“无”)
有
有
影响.(3)第二小组设计的方案:称取10g样品,放入足量的稀硫酸中,欲计算该样品中氧化铜的质量分数,还需测定的一种数据是
充分反应后剩余固体的质量
充分反应后剩余固体的质量
.