摘要:油脂的物理性质 见P195 [想一想]为什么衣服上油渍用酒精比用水易清洗? 因为油脂易溶于有机溶液剂.
网址:http://m.1010jiajiao.com/timu3_id_246796[举报]
 (2012?闸北区二模)苯甲酸甲酯是一种重要的工业原料,某化学小组采用如图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯.有关物质的物理性质见下表所示:
(2012?闸北区二模)苯甲酸甲酯是一种重要的工业原料,某化学小组采用如图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯.有关物质的物理性质见下表所示:| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g?cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
在圆底烧瓶中加入0.1mol苯甲酸和0.4mol甲醇,再小心加入3mL浓硫酸,混匀后,投入几粒沸石,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)甲装置的作用是:
冷凝回流
冷凝回流
;冷却水从b
b
(填“a”或“b”)口进入.(2)化学小组在实验中用过量的反应物甲醇,其理由是:
该合成反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇投料量提高产率,提高苯甲酸的转化率
该合成反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇投料量提高产率,提高苯甲酸的转化率
.Ⅱ粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制.

(3)试剂1可以是
B
B
(填编号),作用是洗去苯甲酸甲酯中过量的酸
洗去苯甲酸甲酯中过量的酸
.A.稀硫酸 B.碳酸钠溶液 C.乙醇
(4)操作2中,收集产品时,控制的温度应在
199.6
199.6
℃左右.(5)实验制得的苯甲酸甲酯精品质量为10g,则苯甲酸的转化率为
75.3%
75.3%
.(6)本实验制得的苯甲酸甲酯的产量低于理论产量,可能的原因是
C
C
(填编号).A.蒸馏时从100℃开始收集产品 B.甲醇用量多了
C.制备粗品时苯甲酸被蒸出.
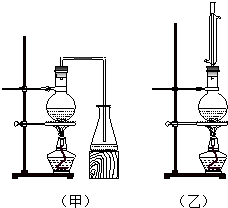 实验室制取乙酸丁酯的实验装置有如图甲、乙两种装置可供选用.
实验室制取乙酸丁酯的实验装置有如图甲、乙两种装置可供选用.制备乙酸丁酯所涉及的有关物质的物理性质见下表:
| 乙酸 | 1-丁醇 | 乙酸丁酯 | |
| 熔点(℃) | 16.6 | -89.5 | -73.5 |
| 沸点(℃) | 117.9 | 117 | 126.3 |
| 密度(g/cm3) | 1.05 | 0.81 | 0.88 |
| 水溶性 | 互溶 | 可溶 (9g/100g水) |
微溶 |
(2)该实验生成物中除了主产物乙酸丁酯外,还可能生成的有机副产物有(写出结构简式)
(3)酯化反应是一个可逆反应,为提高1-丁醇的利用率,写出两种可行的方法:
①
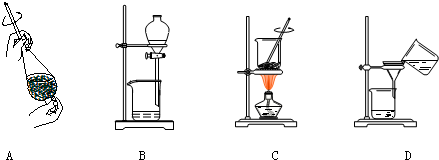
(4)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是
(5)有机物的分离操作中,经常需要使用分液漏斗等仪器.使用分液漏斗前必须
几种常见晶体的物理性质见下表,请完成表中空格
(1)金刚石的同素异形体是
(2)上述晶体中熔化成液态时无需破坏化学键的是
(3)金刚石和二氧化硅硬度大、熔点高的主要是因为晶体中的原子以共价键结合成
查看习题详情和答案>>
| 晶 体 | 氯化钠 | 氯化钡 | 金刚石 | 二氧化硅 | 硫 | 白磷 | 钠 | 钨 |
| 熔点 0C | 801 | 1560 | 3550 | 1723 | 112.8 | 44.1 | 97.8 | 3410 |
| 硬 度 | 较 硬 | 较 硬 | 很 硬 | 硬 脆 | 脆 | 软 | 柔 软 | 硬 |
| 晶体类 型 | ||||||||
石墨
石墨
(2)上述晶体中熔化成液态时无需破坏化学键的是
分子晶体
分子晶体
,从熔点、硬度看规律性最差的是金属晶体
金属晶体
,晶体中存在分子的是分子晶体
分子晶体
(本小题各空匀填写晶体类别)(3)金刚石和二氧化硅硬度大、熔点高的主要是因为晶体中的原子以共价键结合成
空间网状结构
空间网状结构
.二氧化硅和二氧化碳都是ⅣA族元素的氧化物但它们的物理性质相差很大,这主要是因为它们的晶体类别
晶体类别
不同.由分子构成的物质,影响其熔沸点和溶解度的重要因素之一是范德华力
范德华力
.(2008?闵行区模拟)在高中阶段,我们学习了两种酯的实验室制备方法:
①乙酸乙酯的制备(装置如图1);
②乙酸丁酯[CH3COO(CH2)3CH3]的制备(装置如图2).

制备这两种酯所涉及的有关物质的物理性质见表:
请回答下列问题:
(1)在乙酸乙酯的制备过程中,采用水浴加热的优点为
(2)乙酸乙酯制备时,饱和Na2CO3溶液的作用是
A.上口倒出 B.下部流出 C.都可以
(3)在乙酸丁酯制备中,下列方法可提高1-丁醇的利用率的是
A.使用催化剂 B.加过量乙酸 C.不断移去产物 D.缩短反应时间
(4)1-丁醇若含有乙醇,有同学认为制得的乙酸丁酯中含有乙酸乙酯.为了证实该观点,可尝试选用下列

查看习题详情和答案>>
①乙酸乙酯的制备(装置如图1);
②乙酸丁酯[CH3COO(CH2)3CH3]的制备(装置如图2).

制备这两种酯所涉及的有关物质的物理性质见表:
| 物理性质 | 乙酸 | 乙醇 | 1-丁醇 | 乙酸乙酯 | 乙酸丁酯 |
| 熔点(℃) | 16.6 | -117.3 | -89.5 | -83.6 | -73.5 |
| 沸点(℃) | 117.9 | 78.5 | 117 | 77.06 | 126.3 |
| 密度(g/cm3) | 1.05 | 0.79 | 0.81 | 0.90 | 0.88 |
(1)在乙酸乙酯的制备过程中,采用水浴加热的优点为
受热均匀,易控制温度
受热均匀,易控制温度
;制备乙酸丁酯的过程中,直玻璃管的作用是冷凝回流
冷凝回流
,试管不与石棉网直接接触的原因是防止加热温度过高,有机物碳化分解.
防止加热温度过高,有机物碳化分解.
.(2)乙酸乙酯制备时,饱和Na2CO3溶液的作用是
除去乙酸乙酯中的乙酸和乙醇,降低乙酸乙酯的溶解度,便于分层
除去乙酸乙酯中的乙酸和乙醇,降低乙酸乙酯的溶解度,便于分层
.两种酯的提纯过程中都需用到的关键仪器是分液漏斗
分液漏斗
,在操作时要充分振荡、静置,待液体分层后先将水溶液放出,最后将所制得的酯从该仪器的A
A
(填序号).A.上口倒出 B.下部流出 C.都可以
(3)在乙酸丁酯制备中,下列方法可提高1-丁醇的利用率的是
B、C
B、C
(填序号).A.使用催化剂 B.加过量乙酸 C.不断移去产物 D.缩短反应时间
(4)1-丁醇若含有乙醇,有同学认为制得的乙酸丁酯中含有乙酸乙酯.为了证实该观点,可尝试选用下列
C
C
(填序号)装置来做实验,请简述与实验结论有关的实验过程和现象将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液
将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液
.
苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应和水解反应的原理,可以进行苯甲酸甲酯的合成和皂化反应。有关物质的物理性质见下表所示:
| | 苯甲酸 | 甲醇 | 苯甲酸甲酯 |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
相关的实验步骤为:
第一步:将过量的甲醇和苯甲酸混合加热发生酯化反应
第二步:水洗提纯
第三步:蒸馏提纯
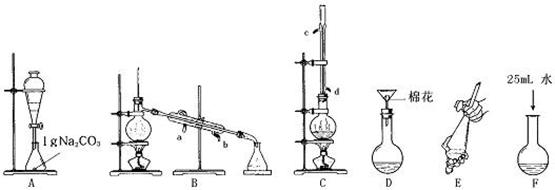
|
(2)C装置中除了装有15g苯甲酸和20mL过量的甲醇外还需要 , ___ 。
(3)C装置中冷凝管的作用是 ,A装置中固体Na2CO3作用是 。
Ⅱ.苯甲酸甲酯的皂化反应
 G H I
G H I(4)能说明G装置中反应完全的现象是 。
(5)在Ⅱ中得到白色固体的质量为5g。假设反应I和反应Ⅱ中:蒸馏提纯的效率为66.7%,加浓盐酸苯甲酸钠生成白色固体的转化率为80%,酯化反应中苯甲酸的转化率为X。其他步骤的转化效率为100%。则X== 。 查看习题详情和答案>>